摘要
真菌的营养部分菌丝体正作为天然、可持续且可生物降解材料的先锋发明,应用于广泛应用。它们由一个自生长且相互连接的细长细胞纤维网络组成,其化学和物理性质可根据生长条件和所摄取的底物进行调整。迄今为止,只有菌丝体提取物及其衍生物被评估和测试,用于生物医学应用。本研究将可食用真菌Pleurotus ostreatus 和灵芝 菌丝体的整个纤维结构呈现为自生长的生物复合材料,模仿人体组织的细胞外基质,理想地作为组织工程生物支架。为此,两种菌丝菌株在生长后通过高压菌灭活,研究其形态、细胞壁化学组成以及流体力学和力学特征。最后,研究其生物相容性及与原发人类真皮成纤维细胞的直接相互作用。研究结果展示了菌丝体作为全天然且低成本的生物支架的潜力,是现有组织工程系统的替代方案。
介绍
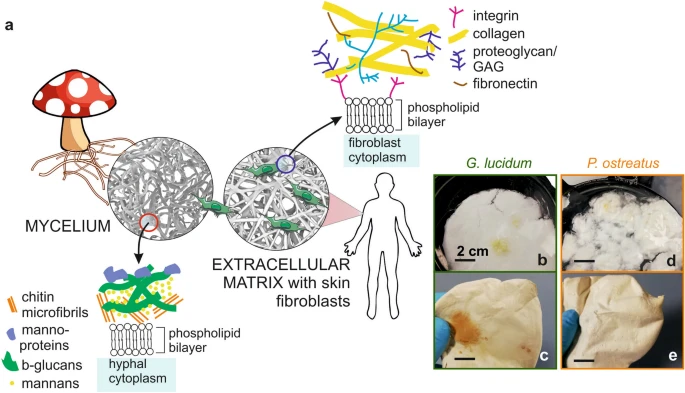
细胞外基质(ECM)由多个大分子组成,其作用是为器官和组织中的细胞提供物理支持、通信通路和三维组织(见图)。1a) 1,2.ECM在孔隙度、机械性能和生化附着线索方面存在差异,这取决于其所支持的细胞类型和所处组织3.在过去几十年里,组织工程领域已有多项努力试图模仿这种多样性,并开发出支持人类组织再生的特定工具。因此,设计了多种支架材料,电纺、冻干和3D打印等技术被开发并广泛应用。这些自上而下的方法允许精细且精确地制造合适的多孔结构,但需要使用溶剂和复杂的仪器 4,5,6.电离丝从许多天然材料(如丝绸)中生成排列整齐的微米和纳米级纤维垫 7,8,角蛋白9,10,11,海藻酸盐 12,13,千岁先生14,胶原蛋白15)和合成(例如PLA16,PCL17,PVP18,以及PEO19通过对初始聚合物溶液施加高压来实现聚合物:尽管正在试验环保溶剂,但为了达到适合纤维形成的粘度和浓度,仍可能需要使用有毒试剂20,21,22.同样,粘弹性特性是3D打印墨水的关键因素,导致使用潜在有害化合物,同时使用昂贵的3D打印机以确保高分辨率 23,24.另一方面,水是冻干技术中最主要的溶剂,其主要缺点在于控制升华步骤时使用昂贵设备25.
菌丝体作为潜在的生物支架材料。(a )真菌菌丝体和细胞外基质的显微结构和细胞组成的示意图,强调其外膜成分。(b –d )照片显示了两种菌丝体在未进一步治疗(b –d )和高压灭菌后(c –e )生长后的宏观特征。 结合这些技术进步,生物聚合物的引入确保了功能性和智能脚手架生产的重大进展。生物聚合物如PCL和PLA成功满足了可生物降解材料的需求,同时具有延长寿命和体内机械耐受性。另一方面,这些合成聚合物中的化学基团无法主动促进细胞相互作用 26,27.
多糖和蛋白质聚合物,如几丁质28,海藻酸盐29透明质酸 30,31,丝绸 32,33,以及角蛋白9显示细胞迁移的生化指导,克服上述合成聚合物常见的附着靶向不足问题34.事实上,蛋白质基生物材料中多糖中的羟基和纤维内青素特异性氨基酸序列(RGD:精氨酸-甘氨酸-天冬氨酸,LDV:亮氨酸-天冬氨酸-缬氨酸)已被证明对细胞粘附的成功至关重要 35,36.植物来源的蛋白质和多糖已被证明比动物性蛋白更可持续且成本更低,克服了提取和资源回收中的一些问题37.然而,稳定且防水的支架只能通过交联或混合步骤获得38,39,40.
因此,将合适的三维结构、合适的机械抗性和能够稳定且主动维持细胞附着的生物功能基团结合在一起,仍然面临巨大挑战。近年来,动物和植物组织的去细胞化被提出作为解决这一问题的有效方法,但要实现细胞生长和附着所需的支架,仍需采取多种物理、化学或酶类处理的前置步骤 41,42.
真菌的营养部分菌丝体正逐渐成为一种高度可调、自生长、可生物降解且成本低廉的生物材料。迄今为止,它已被用于包装、纺织和建筑等领域的探索性应用43.菌丝体由细长的细胞组成,称为菌丝,这些细胞从生长基质中膨胀吸收养分,并自发生长在纤维状的垫子中。本研究中讨论的食用真菌品种明灵芝和Pleurotus ostreatus即属此类44.总体而言,菌丝体呈现自生长的多孔结构,其菌丝外膜同时暴露多糖和蛋白质(图。1a)。此外,在我们之前的研究中,报告指出菌丝体的形态、化学成分、流体力学和力学性能可以通过改变真菌菌株及其生长基质来精细调节45,46,47.
迄今为止,科学研究报告了菌丝体在生物医学应用中的应用或其衍生物生物相容性研究。事实上,有几种真菌菌株被报道会分泌生物活性多糖,主要是几丁质衍生物,这些多糖可以从培养基中提取,也可以直接从菌丝网络中提取,使用强碱或强酸48.仅通过铸造这些提取物产生的膜,如Su等人报道的Saccachitin。49以及Chien等人生产的根突蛋白。50显示出对成纤维细胞和角质细胞生长的积极影响。据我们所知,只有Narayanan等人的工作报道了将曲霉属用作人类角质细胞培养支架的案例,但这种应用只有在对菌丝体进行β-尣基乙醇强力化学处理后才得以实现51.在这里,我们首次试图展示如何直接利用整个真菌菌丝结构,无需化学预处理,作为一种有效且可持续的全天然、自生长且低成本生物医学支架受控制造的替代方案。因此,我们介绍了灵芝(Ganoderma lucidum)和Pleurotus ostreatus mycelia作为组织工程粘附平台的生长与特性,并报告了它们作为主要人类细胞模型生物相容性的初步但有希望的结果。
材料与方法
1、菌株、培养基与生长条件
灵芝DSM9621和Pleurotus ostreatus DSM11191活性培养物从德国DSMZ购买,并在100毫米培养皿中保存,培养基为马铃薯葡萄糖汤(PDB,默克),每30天将培养基转移到新鲜培养基。一块20天生长的菌丝体被接种在含有30毫升PDB的100毫米培养皿中,水含量为24克/升。介质在使用前由SYSTEC-VX 40在120°C高压灭菌处理,持续20分钟。菌丝体在气候室(Memmert,HPP 260)中孵育,温度为27°C,相对湿度78%,且在黑暗中。
2、材料制备
生长20天后,当整个板面被覆盖后,收集菌丝体,用刮刀和去离子水从基质上清洗。菌丝体随后在烤箱中以50°C干燥15小时,或在120°C高压灭菌20分钟。高压灭菌菌丝体随后在层流式熏蒸罩下干燥,并用紫外线照射约100分钟。
3、SEM和TEM分析
菌丝体在2%戊二醛溶液中固定,置于0.1 M cacodylate buffer中,室温下2小时。在同一缓冲液中多次清洗后,样品在1%四氧化锇中与MQ水后固定2小时,并用MQ水清洗。菌丝体随后在乙醇浓度上升的水溶液中(30%至100%)、1:1乙醇(HMDS,Sigma-Aldrich)和100%HMDS中进行10分钟的脱水,并在空气中过夜干燥。最后,样品用10纳米金层溅射,并使用配备钨丝、以10千伏加速电压运行的JEOL JSM-6490LA扫描电子显微镜(SEM)进行分析。
TEM分析中,如前述描述,先用戊二醛固定后,菌丝体在1%四氧化锇中置于MQ水中2小时,再用MQ水洗涤,并在4°C水溶液中染色过夜。随后,样品在分级乙醇系列中脱水,并在70°C下浸渍48小时。 约70纳米的截面52用钻石刀在徕卡EM UC6超切片机上切割。透射电子显微镜(TEM)图像使用配备2毫秒电荷耦合装置相机的Jeol JEM 1011(日本Jeol)电子显微镜采集。
4、密度与孔隙度
骨骼密度通过热科学Pycnomatic Evo氦态测量测量,直径为44厘米3密室。测量在20°C进行。 真实(或骨架密度)是指样品体积所指的样品质量,排除所有孔隙和空隙体积,但考虑了“封闭”孔隙(即材料内部任何气体无法进入的空腔)。骨骼密度通过检测密封且压力平衡的腔体内氦气体积变化来测量。氦是一个微小的原子,可以渗透到固体中极窄的孔隙,从而确定该固体所占的真实体积。干燥质量与体积的比值决定了被测材料的真实密度。每个样本均值十项测量。孔隙度通过使用Pascal 140 Evo和Pascal 240 Evo汞孔隙测量仪(Thermo Scientific)进行的汞侵入孔隙测量(MIP)测定。在这种技术中,样品完全被汞嵌入。然后压力增加,使汞开始进入孔隙。总孔隙度(由MIP估计)与测量结束时完全侵入的汞体积有关。孔隙度实际上表示为孔隙体积(内腔体积)与外部样品体积的比值,而孔径分布则取决于每个压力范围内侵入的汞体积。汞侵入压力设定为0.0136兆帕,并持续增加至200兆帕,速率为每分钟6至14兆帕−1.汞与样品的接触角和纯汞的表面张力被假定为140°和0.48牛顿米−1,分别。使用洗燃方程计算了施加压力下的孔径,假设孔隙为圆柱形45.
5、化学分析
样品的红外光谱通过衰减全反射(ATR)附件(MIRacle ATR,PIKE Technologies)与傅里叶变换红外分光光度计FTIR光谱仪(顶点70伏FT-IR,Bruker)结合获得。所有光谱记录在3800至600厘米之间−1,直径4厘米−1分辨率,累计64次扫描。样品轻轻放置在ATR配件的一点上,缓慢压制,使该部分与基底接触生长(称为“底部”),并置于ATR晶体上。为确保获得光谱的可重复性,每种类型各测量三个样品45.光谱分析使用Origin pro 2016软件完成。
6、流体动力学表征
接触角(CA)量角仪(DataPhysics OCAH 200)用于室温静态水接触角测量。在相应表面沉积了五微升的水滴,60秒后拍摄了水滴的侧面图像。CA通过拟合捕获的水滴形状自动计算。在随机位置对每个样本进行了多达15次接触角测量,报告了其平均值和标准差45.接触角是在干燥或潮湿环境下进行调控后测量的(即在100%相对湿度下调制24小时)。为了取水,干样品会用灵敏的电子天平称重,然后放入不同的湿度箱中。样品通过干燥器干燥24小时,称重后在100%湿度条件下转移24小时,再进行称重。吸附水量是根据初始干重计算的。
7、机械表征
样品被切割成20×35毫米2并在室温下测试,经过24小时、100%相对湿度调节。拉伸应力曲线由双柱通用测试机(Instron 3365)获得:样品安装在机夹上,并以每分钟1毫米的速度变形直到失效。杨氏模量E、极极拉伸强度终极超速和断裂伸长均从应力-应变曲线中提取45.存储模量E’和tanδ(即损耗与存储模数的比值,代表相对能量耗散)也用Q800 DMA测试机(TA仪器)在单轴拉伸模式下测量,施加振幅为20微米、频率为7、10和16赫兹的正弦变形45.
8、菌丝体提取物特征
(1)体外生物相容性
使用原级人类真皮成纤维细胞(HDFa,Thermo Fisher Scientific)作为细胞模型,研究生长菌丝体的生物相容性。在T75瓶中培养,培养基106并补充LSGS套件(Thermo Fisher Scientific)后,细胞以7000细胞/厘米密度播种到24孔板上2并在37°C、5%CO的孵育箱中过夜附着2.P. ostreatus和G. lucidum提取物的制备方法如下。高压灭菌菌丝体切成约20毫克的块,在紫外线下消毒20分钟(每边10分钟)。为去除真菌基质中多余的PDB,这些片段浸入无菌磷酸钾缓冲液(PBS,pH 7.4,Gibco),并在37°C下培养24小时。又用新鲜的PBS进行了第二次洗涤,持续了24小时。随后,每个20毫克菌丝体片段与1毫升106培养基一起孵育24小时,利用所得的存液制备测试稀释液(1:2、1:3、1:4、1:20、1:40、1:100)。连接的HFDa细胞(在4–6次传代处)用菌丝提取物处理24、48和72小时,而在正常培养基106+自然格培养基中培养的细胞则作为对照。MTS测定(CellTiter 96 AQ®乌乌斯进行了一次溶液细胞增殖测定(Promega)以确定细胞存活能力。简而言之,所有样本均在新鲜培养基(500微升)中孵育,每孔加入25微升试剂。潜伏3.5小时后,记录到490纳米的吸收读数。三次独立实验以三份形式进行。假设方差不等,学生t检验进行了,考虑p<0.01值。
为进一步评估菌丝基质的生物相容性,进行了半接触测定。原发人类成纤维细胞(通道4–6)被种子植入24孔板上,密度为7000细胞/厘米2然后让它过夜附着。P. ostreatus和G. lucidum被切成小块(重量在1到5毫克之间),并按照前述方式清洗和灭菌。次日早上,补充新鲜培养基(1毫升),并在每个孔中轻轻浸入一小块菌丝体,并让其漂浮24、48和72小时。随后,基质被小心取出,注意不扰动井底连接的细胞层,随后进行了MTS测定。三次独立实验以三份形式进行。假设方差不等,学生t检验考虑p<0.01值。
为了观察受各种处理的成纤维细胞形态,细胞被以5000细胞/厘米密度的玻璃覆盖片镀膜2并如上所述处理。随后,用预热的PBS清洗细胞,并用3.7%对甲醛固定20分钟。使用DAPI溶液(2.5 μg/mL)染色细胞核(在黑暗中15分钟)。为了使肌动蛋白纤维染色,成纤维细胞在Alexa Fluor 488 Phalloidin(Thermo Fisher Scientific,PBS中1:100稀释)中潜伏20分钟,先用0.3% Triton X-100渗透(8分钟)。准备好的封面片随后用Fluoromont-G安装在玻片上,并用尼康A1共軛焦显微镜进行成像。
(2)P. ostreatus 基质上的细胞板
为了研究菌丝体作为细胞附着和生长底物的适宜性,人类初级成纤维细胞被用作一个具有挑战性的平台。简而言之,菌丝体矩阵被切成直径1厘米的圆形块并进行消毒/清洗,如前一段所述。底物置于24孔板底部,并用无菌PDMS环固定(外径=1.5厘米,内径=0.8厘米)。部分基质在37°C下与400微升纤维联素(20 μg/mL,纤维内联蛋白人类蛋白,Thermo Fisher Scientific)培养1小时,其他基质则未涂覆,并培养在无菌PBS中。去除纤维联素/PBS后,基质在无菌罩下干燥2小时,并以密度为5000细胞/厘米的细胞播种2.培养48小时后,样品被固定在3.7%的对甲醛中。为部分阻断真菌底物的自体荧光信号,所有染色溶液(DAPI和Alexa Fluor 546 Phalloidin)均用1%牛血清白蛋白制备,并按上述方法处理样品。彩色和玻璃安装基底用尼康A1共焦显微镜成像,配备560纳米激光。图像采用PMT和光谱探测器(光谱采集范围为541至679纳米,光栅分辨率为6纳米)进行拍摄。图像分析(光谱解混、投资回报率定义和光谱剖面)使用ImageJ(https://imagej.nih.gov)完成。
(3)P. ostreatus细胞支架的SEM成像
如前所述,P. ostreatus基质如前所述,并用HDFa细胞播种48小时,经过上述处理,并由配备钨丝、在10 kV加速电压下运行的JEOL JSM-6490LA扫描电子显微镜观察。
(4)高分辨率UPLC质谱仪
样品在氮气下干燥后,在水中用10%丙腈重新合成。随后,将5微升样品注入Acquity UPLC液相色谱系统,配合Synapt G2 QToF高分辨率质谱仪(均来自美国马萨诸塞州米尔福德Waters)。分析物随后在BEH(2.1×100毫米)反相柱(Waters)上使用水中丙烯腈的线性梯度(5%至100%)分离。洗脱化合物通过高分辨率质谱法在正负离子电喷雾模式下进行了分析。使用亮氨酸-恩克法林参考标准作为锁质量,以实现质量精度低于5 ppm。代谢物通过查询公开的HMDB(人类代谢组数据库)和LipidMaps参考数据库进行了初步鉴定。
结果与讨论
1、菌丝的生长、采集与灭活
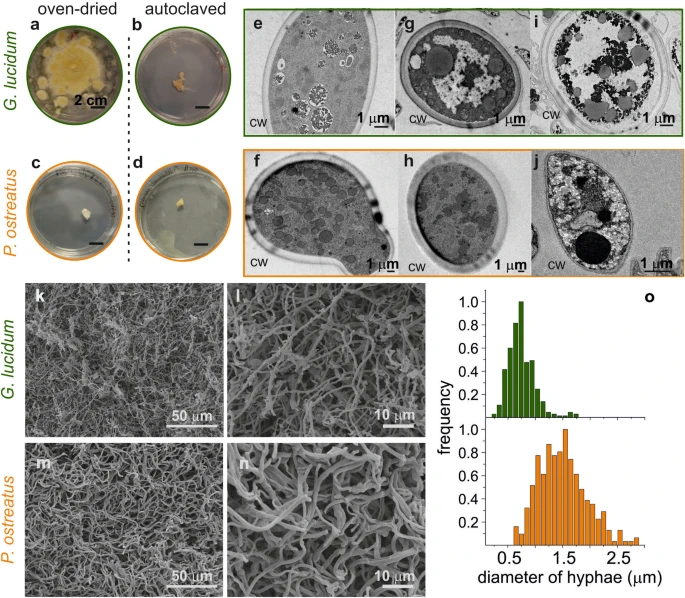
真菌菌丝体被种植在装有马铃薯葡萄糖汤(PDB)的培养皿上,置于气候室(27°C,78% R.H.)内,直至完全覆盖表面,然后收集并从基质中清洗(见图)。1b–-e)。收获后,完全失活菌丝体的生物活性以阻止其生长,是测试其作为潜在生物材料支架的第一个关键步骤。菌丝体失活通常通过热处理完成53.然而,在一项对照实验中,将50°C烘干的菌丝体片段重新与PDB接触,灵芝偶尔会重新生长,这与Pleurotus不同(图)。2a,c),表明这种弱处理可能不足以实现稳定构型。这一现象并非完全意外,因为灵芝菌株的耐热性已被观察到54与Pleurotus ostreatus相反55.因此,选择高压灭菌器作为生长后处理,因为两种菌株在接触后都显得无效(见图)。2b,d)。透射显微镜(TEM)检查显示,烤箱处理后(见图)。2g,h),其内部细胞组织与对照组相当(见图。2e,f)。相反,在高压灭菌(见图)之后菌丝细胞的含量发生了剧烈变化:细胞内部出现了大面积白色区域,可能是由于质溶作用,热压冲击下形成了液泡56.重要的是,主要结构成分细胞壁(CW)在两个菌丝体中仍然完整,尽管胸膜肌壁略有收缩。细胞直径在烘干和高压灭菌菌丝体之间相当,表明通常报告于强热处理真菌时出现的细胞收缩,但在此情况下不会发生57.基于这些结果,进一步分析仅对高压灭菌样本进行了。
菌丝体的形态特征。(A –D )“再生”实验,使用烤箱干燥和高压灭菌丝体(e –j )进行TEM成像,分别是菌丝体生长(e 、f )、烘烤干燥(g 、h )和高压灭菌(i , j ),CW = 细胞壁 。(k,n ) 高压灭菌丝体的SEM图像;(o )通过高压菌丝体的SEM图像计算出的菌丝直径分布。 2、形态特征
扫描电子显微镜(SEM)对高压灭菌后菌丝体的观察使得菌丝结构的观察和直径计算得以实现(见图)。2k–n),这两者都是生物医学支架的必备特征。纤维呈随机定向,菌株表现出与Haneef及其同事在烘干菌丝中观察到的形态差异相同46.在灵芝中,可见两种菌丝结构,一种管状短结构,另一种较长且光滑的,定义为线状。相反,Pleurotus ostreatus mycelia 仅由后者组成。菌丝直径分布与此前报道的烘干菌丝体相当:胸襟菌丝体较大,平均尺寸为1.5 ± 0.4微米,而灵芝丝状菌丝体平均为0.7±0.2微米(见图)。20)。这种纤维状网络排列和尺寸已被报道适合细胞附着58,59,60.
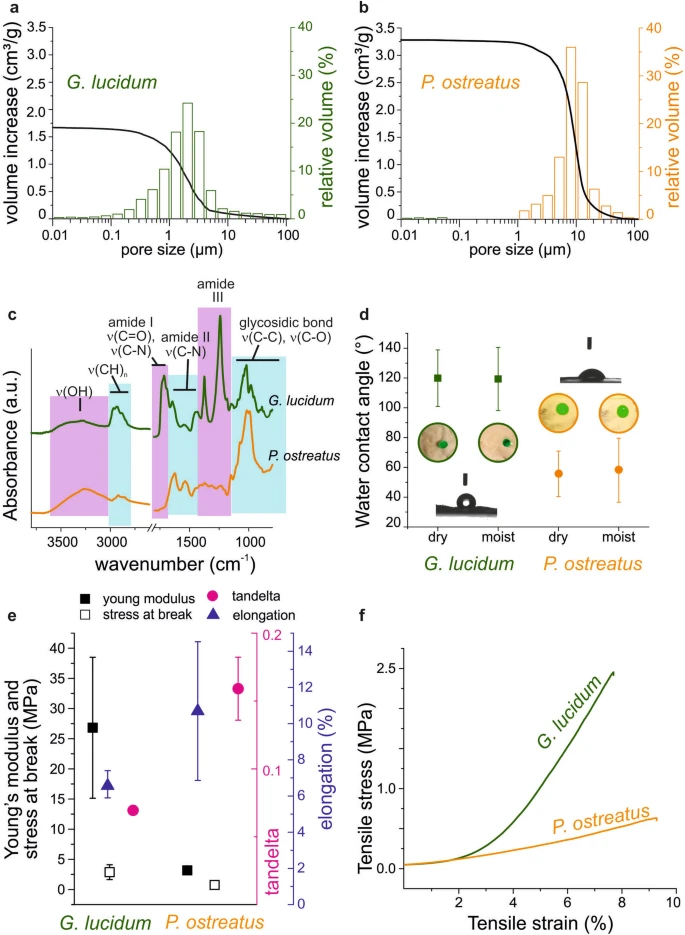
孔隙度能够极大影响细胞迁移、氧气调节和养分交换,因此在支架设计中应考虑的一个关键参数61.通常,在组织工程应用中,平均孔径通过SEM显微照片的后处理测量,而总孔隙度则可通过液态置换法单独计算,通常使用乙醇47,62,63.本研究通过汞侵入孔隙测量(MIP,见实验方法部分)分析推断了总孔隙率和孔径分布,以确保能够涵盖这些天然且高度变异材料所呈现的全部尺寸范围(见图)。3a–-b)。特别地,总孔隙度的确定依赖于侵入的汞总体积(图中的黑色曲线)。3a, b),而不同孔径的信息则根据每次压力下侵入的体积(图中的柱)计算。3a, b)。为避免MIP特征高压下孔隙开口的假阳性,分析前采用氦微型测量测量骨骼密度64.骨密度是指样品干重与样品体积(不含所有开放孔隙)之间的比值。由于原子极小,氦能够测量更小的孔隙,在软材料(如菌丝体)中出现伪影的风险更低 65,66.
菌丝体的孔隙性、化学性、流体力学和机械特征。(a , b )通过MIP测量孔径分布(柱)和总孔隙率(曲线);(c )两个菌丝体的ATR-FTIR光谱;(d ) 干燥和湿润菌丝体的接触角。插图:两种菌株的菌丝体上有彩色水滴,干水或湿水。滴液体积为5微升。(e )杨模量、断裂应力和拉伸试验后的伸长结果;DMA分析后的tanδ值。(f )研究中两个菌丝体的拉伸测试曲线。 Pleurotus 3D网络的密度更高(1.48 ± 0.03 g/cm3)比灵芝(1.34 ± 0.02 g/cm)高于3;未显示数据),且其整体孔隙度(85%)高于其对应模型(68%)。孔径分布显示,灵芝的大部分汞侵入在1至5微米之间的孔隙中,而Pleurotus则在7至20微米的孔洞中。总体而言,这些发现表明不同菌丝网络可能根据菌丝结构和整体孔隙度,承载特定细胞类型或细胞簇。特别是,考虑到本初步研究的范围,成纤维细胞更能更好地渗透呈现20至100微米孔径的支架,但较小孔隙更有利于细胞的粘附、桥接和ECM产生60,67,68.
3、菌丝体的化学组成
菌丝体表面存在多种化学功能,使其成为组织工程应用的有趣平台。细胞通常通过与细胞外基质(ECM)中存在的众多蛋白聚糖和蛋白质相互作用,从而附着在碳水化合物和蛋白质基层上。特别是糖胺聚糖表现出的羧基、硫酸基和羟基,以及ECM蛋白(如胶原蛋白和纤维神经素)上出现的氨基酸RGD基序,是细胞附着的主要原因69.通常,用于脚手架生物制造的高分子和生物材料并不自然展现上述所有化学功能,这些功能必须在第二步中添加到脚手架表面。例如,纤维素可以通过磷酸化以提高其生物相容性,而聚合物电纺纤维则可以通过硫酸化合物富集70.ATR-FTIR分析(图:3c)自生长材料揭示了羟基、羧基和酰胺基团在两种菌株中都存在的原因,因为真菌细胞壁由多糖、脂质和蛋白质组成(见图)。1a)71,72,73.两种研究株在ATR-FTIR光谱上的主要差异在于酰胺键拉伸面积。灵芝菌丝体有一个峰,1715厘米−1(伸展区)以及两个峰峰,分别位于1375厘米和1240厘米−1(酰胺III拉伸范围),这些在Pleurotus光谱中不可见。另一方面,后者在1620厘米和1540厘米处有两个山峰−1(酰胺II拉伸范围),与灵芝谱不同,灵芝光谱仅有一个峰值,位于1450厘米−1在同一区域内可见。这些范围的差异与几丁质含量的变化有关,而这对菌丝体的特性(如疏水性和机械抗性)有很大影响46.如前所述,细胞最好附着在碳水化合物和蛋白质基层上69.因此,真菌表面观察到的多种化学功能为组织工程开发完全基于真菌的生物材料提供了有前景的道路。
4、流体动力学表征
形成的高压菌丝体的流体动力学行为通过静态水接触角(CA)以及在饱和水大气中吸附水分的能力来表征。在干燥和潮湿环境中对菌丝基底进行24小时调控后测量了接触角,因为本研究第二部分考虑了含水介质中的应用(见图)。3d)。灵芝在两种条件下都显示出稳定的CA为≈119°。同时,灵芝菌丝体吸附受水能力有限,因将材料置入潮湿腔室后仅记录到30±1%的重量增加(数据未显示)。另一方面,Pleurotus 菌丝体在两种条件下CA值较低,即干菌丝体CA为56±15°,湿润菌丝体为58 ± 21°。这些菌丝体更容易吸附水分,在潮湿腔室中24小时后,菌丝体数值可增加68±6%的重量。
上述化学成分和孔隙度的差异可以解释其多样的流体动力学行为,尤其是在水分吸收方面。此外,所得的水接触角强烈依赖于整个地表地形 74,75.一般认为,亲水性更高的表面更有利于细胞附着76但研究表明,蛋白质甚至可以附着在更疏水的表面77尤其是在增加种子细胞数量或培养时间后78,79,80.因此,水动力学特性的多样性并不排除任何菌丝体在进一步测试生物相容性和细胞附着适宜性之外。
5、机械表征
在人体内部,组织刚度范围为kPa–MPa,细胞根据基底的机械性质分化、生长和对环境作出反应81.菌丝体在干燥状态下是脆性材料,这一特性使得它们在复合材料中结合,用于建筑、热/声学隔离和设计制造82,83,84.因此,鉴于菌丝体固有的纤维性质,获得其精确的机械性质测量可能具有挑战性85.因此,机械性能研究通过拉伸测试和动态机械分析(DMA,见图)进行。3e, f)。菌丝体在测量前需在湿润大气(100% RH)中进行调理,正如这里设想的湿应用。明心灵芝的杨氏模量为26.8±11.7 MPa,伸长度较小,为6.6±0.8%,相较于Pleurotus ostreatus,杨氏模量为3.2 ± 0.1 MPa,伸长率为10.7±3.8%。相反,断裂时记录的应力仅有细微差别,即灵芝为2.9±1.2兆帕,Pleurotus为0.7±0.3兆帕。结合这些结果和计算出的棕褐-δ值,灵芝菌丝体看起来更硬,而Pleurotus则更具延展性。总体而言,菌丝体的刚度与组织工程中其他材料报告的数值相当,尤其是在皮肤模拟方面 60,86.特别是菌丝体的机械性质在微米尺度上与活体组织中测量的性质极为相似,有利于体外细胞的粘附和组织形成 87,88.
6、人类原发性真皮成纤维细胞对真菌菌丝体的反应
(1)生物相容性测定
多种真菌材料衍生物此前已被测试其维持细胞生长的能力。某些真菌菌株(如灵芝、镰刀菌、曲霉菌))89据报道,它们分泌生物活性多糖(通常是分支杂葡聚糖或糖蛋白),这些多糖可从培养基中获得48,90,91,92.另一方面,直接将强碱或强酸作用于菌丝基质,然后铸造提取的分子,可以制备菌丝衍生物,这些衍生物可作为细胞培养的底物。例如苏氏及其同事报道的Saccachitin,以及Chien等人生产的根基红蛋白,其中从菌丝体提取的几丁质被铸造成膜,作为皮肤替代和成纤维细胞生长的测试对象 49,50或因其免疫调节活性93.
鉴于上述团队取得的良好成果,本项目迈出了一步,将整个菌丝体视为组织生长和修复的潜在支架。因此,通过一种不需使用任何溶剂或机械处理的程序,将保留潜在的治疗效果和菌丝体的三维、类ECM结构,这与Narayan等人对曲霉属的报告不同。菌丝体51.在这项工作中,采集菌丝体后唯一需要的步骤是高压灭菌。
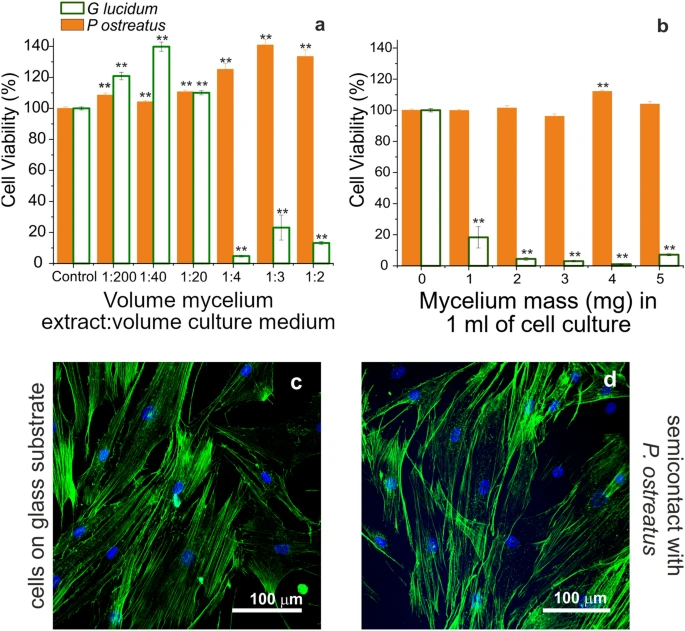
在ISO10993-5标准测试后进行了初步生物相容性调查,该测试评估了整粒菌丝材料细胞培养基提取物的细胞毒性效应。实验对象是原发人类成皮成纤维细胞(HDFa)10.菌丝培养基提取物下培养细胞的存活能力首次通过MTS测定进行评估(见图)。4a 和图 S1a,b )。此外,还进行了“半接触”实验(见图)。4b,图S1c、d),其中附着在24孔板底部的成纤维细胞在一块菌丝体漂浮于其上的情况下进行培养。通过对Pleurotus ostreatus的实验,记录了每种测试病症的最大生存率(见图。4A、B,全橙色条)。此外,这些成纤维细胞表现出与对照细胞相同的形态(补充培养基),通过肌动蛋白染色和共焦显微镜观察可见(见图)。4c, d)。因此,来自Pleurotus ostreatus的菌丝体成为组织工程应用的有前景基底。相反,在灵芝明化样本存在下进行的初步检测显示了不同的趋势:“提取物”实验中,细胞相容性相较对照样本在高稀释(1:200和1:40菌丝体提取物/培养基,v/v)下略有提升,而在更高浓度提取物存在下则显著下降(稀释1:2时可行性达到13.2±0.9%), 无花果。4a,空绿条)。同样,当提取物处理时间较长时,只有提取物的高稀释(从1:200到1:20)不影响细胞存活率(见图S1a,b)。这可能表明在低灵芝明化浓度下存在轻微刺激效应,这需要进一步研究。
对HDFA细胞的生物相容性。(a, b )。在菌丝提取物(a )存在或半接触(b )存在下,24小时后MTS测定的原发性人类成纤维细胞(HDFa细胞)存活率。报告的数值显示了从1毫升含生长因子培养基106中,20毫克菌丝体的浓缩液中制备的稀释液。数据以平均标准误±表示,p < 0.01(**)被视为显著。(c, d )。对照细胞的对照细胞在玻璃基底上被镀膜,并用含生长因子(c )的培养基106处理,或与5毫克的P. ostreatus (d )半接触的对照细胞的共焦点图像。 然而,当灵芝碎片直接放入培养井24小时时,成纤维细胞未能存活。为了了解这一结果的可能解释,采用高分辨率UPLC-MS(超高性能液相色谱-质谱)分析了两种菌株的提取物。该实验显示,即使经过两次24小时无菌PBS洗涤步骤,仍发现了显著量的灵芝代谢物。这种代谢物(甘顺性质V,一种高含氧的拉诺斯坦型三萜类,见图S2)已知具有凋亡和细胞毒性活性 94,95.提取物中还检测到有毒的葡萄糖苷夹竹蒽,这很可能导致成纤维细胞死亡96.另一方面,同样对Pleorotus的分析显示,羟基脂肪酸是主要代谢产物(见图S3),对原生细胞无害。
(2)Pleurotus ostreatus 菌丝体上人类初级成纤维细胞的直接生长
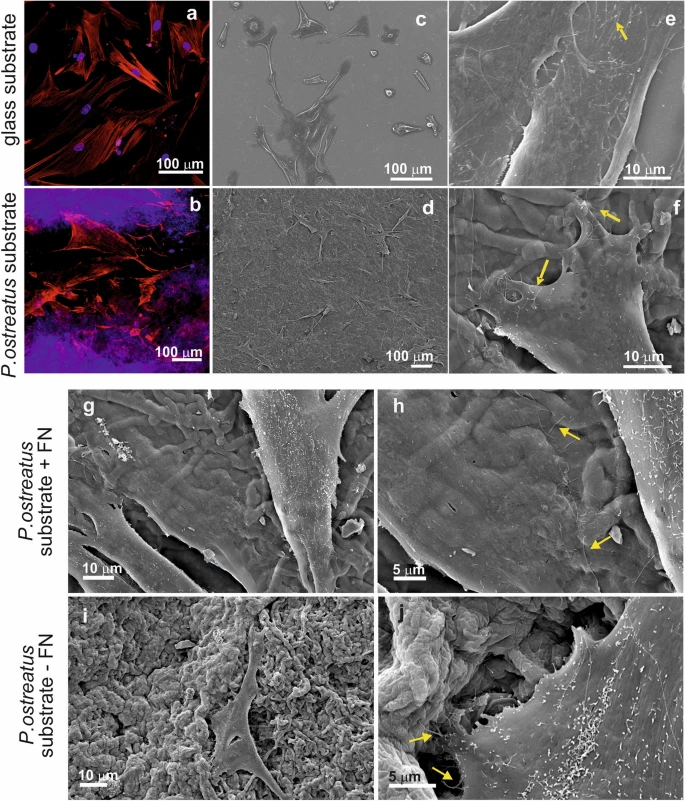
考虑到初步生物相容性结果,原发成纤维细胞的附着仅测试在Pleurotus ostreatus的菌丝体上。实验在纤维素(FN)涂层基底上进行(见图)。5d, f, g, h)或覆盖FN无被膜菌丝体(图。5 i,j),以观察这种已知介导细胞-底物相互作用的ECM蛋白的存在是否是实现细胞附着的必要条件。如共焦(图)。5b)和SEM显微镜中,细胞附着成功,初级成纤维细胞附着在波纹状的三维菌丝基质上,呈现出健康的形态(与FN涂层对照玻璃载玻片相媲美,见图。5a, c, e)。有趣的是,SEM调查揭示了细胞质丝状体(丝足,图中黄色箭头所示)的存在。5f, h, j)从单元的前缘突出。这种现象在Pleurotus ostreatus支架上的细胞中更为明显,无论是FN包裹还是非功能化的,因为丝状体似乎固定在菌丝上。如预期,FN表面功能化时观察到粘附性纤维成细胞的更密实层,表明ECM蛋白涂层对促进初级成纤维细胞附着在Pleurotus ostreatus底物上有用但非必需 97,98.
HDFa细胞在FN涂层玻璃盖片上培养48小时的共焦(a )和SEM显微镜(c 、e )。HDFa细胞在FN涂层P. ostreatus 底物上培养48小时的共焦(b )和SEM显微镜(d 、f )照片。细胞核用DAPI(蓝色可见)染色,肌动蛋白纤维用Alexa Fluor Phalloidin 488染色(绿色高亮)。从附着细胞细胞质延伸出的丝足用黄色箭头表示。(g –j )支架涂层对初级细胞生长的影响。HDFa细胞被播种在P. ostreatus 支架上,骨架上有纤维内联素(g 、h )或未涂层(i 、j )。从附着细胞伸出的丝足用黄色箭头突出显示。 还将开展进一步研究,研究细胞焦点粘附复合体相对于菌丝菌丝结构的分布,并探究菌丝体基材料是否也能积极促进成纤维细胞的生长和迁移99.通过使用高分辨率显微镜和分子生物学工具的研究,或许能更深入地揭示细胞附着于菌丝表面的机制。
结论
总之,具有自发形成三维生物聚合网络的丝状非致病真菌菌丝体,构成了理想的自生长、全天然生物复合物支架用于细胞生长。我们首次证明,Pleurotus ostreatus 的菌丝体可以直接作为细胞生长的支架,从而确定原发人类成纤维细胞的附着,其存活率和形态与对照样本相当。对自生长复合生物材料进行的处理是唯一一种简单快速的高压灭菌工艺,这既能完全灭活真菌孢子,又能通过标准化方法消毒脚手架。据我们所知,这是首次报告原生细胞直接被固定在未改造且功能性不强化的菌丝支架上。另一种丝状真菌灵芝(Ganoderma lucidum )的结果表明,菌丝细胞的完全失活是必要的,但不足以实现生物相容性,因为其水提取物中含有有机酸(甘莧酸V和奥兰甘醇)的picomoral浓度,这对HDFa细胞的存活有害。
总体而言,本文介绍的自生长生物材料的物理化学特征(即 形态、化学成分和润湿性)表明菌丝体作为组织工程可调节平台具有巨大内在潜力。利用特定真菌株与其生长基底耦合产生的不同特性组合,可以为新一代支架设计铺平道路。菌丝体可以被提出作为一种新颖、更可持续的“自下而上”模拟ECM制造方法,是目前用作组织工程支架的其他自上而下和自下而上系统的先进替代方案。我们看到了各种功能性、基于生物复合材料菌丝体的结构,可以设计和应用于生物医学领域的多种应用,从而改变生物材料的构思和制造方式。
参考文献
弗兰茨,C.,斯图尔特,K. M. 和韦弗,V. M.一眼就能看到细胞外基质。细胞科学杂志。 123 (24),4195–4200。https://doi.org/10.1242/jcs.023820 (2010)。
Khoshnood, N. 和 Zamanian, A. 去细胞化的细胞外基质生物墨水及其在皮肤组织工程中的应用。生物印刷 20,e00095。https://doi.org/10.1016/j.bprint.2020.e00095 (2020)。
Stevens, M. M. 和 George, J. H. 探索与工程细胞表面界面。《科学》 310 (5751),1135–1138。https://doi.org/10.1126/science.1106587 (2005)。
Subbiah, R. 和 Guldberg, R. E. 组织工程与再生医学中生长因子递送系统的材料科学与设计原理。高级健康。Mater。 8 (1), 1801000。https://doi.org/10.1002/adhm.201801000 (2019)。
张、Y等。 用于骨骼和软骨组织工程的高分子纤维支架。高级功能。Mater。 29 (36),1903279。https://doi.org/10.1002/adfm.201903279 (2019)。
Doostmohammadi, M., Forootanfar, H. 和 Ramakrishna, S. 再生医学与药物递送:通过电旋生物材料取得进展。科学工程 C 109,110521 。https://doi.org/10.1016/j.msec.2019.110521 (2020)。
皮尼亚泰利,C. 等人。 电纺丝丝纤维用于储存和控制释放人体血小板裂解液。Acta Biomater。 73,365 –376。https://doi.org/10.1016/j.actbio.2018.04.025 (2018)。
Kim, S. H., Nam, Y. S., Lee, T. S. 和 Park, W. H. 丝绸纤维素纳米纤维:电纺丝、性能与结构。Polym. J. 35 (2), 185–190。https://doi.org/10.1295/polymj.35.185 (2003)。
苏阿拉托,G. 等人。 从织物到组织:回收的羊毛角蛋白/聚乙烯基吡咯酮生物复合纤维作为人工支架平台。科学工程 C 116,111151 。https://doi.org/10.1016/j.msec.2020.111151 (2020)。
Kossyvaki, D. 等人。 角蛋白-肉桂精油生物复合纤维贴片用于皮肤烧伤护理。《数学研究 》,1 (6),1805–1816年。https://doi.org/10.1039/D0MA00416B (2020)。
严启昌、陈启怡、黄志英、郭振泰。林,F.-H.通过电纺丝制造角蛋白/纤维蛋白膜,用于血管组织工程。《化学杂志》B4 (2), 237–244。https://doi.org/10.1039/C5TB01921D (2015)。
Hajiali, H. 等人。 海藻酸盐-薰衣草纳米纤维具有抗菌和抗炎活性,有效促进烧伤愈合。《材料化学杂志》 B 4 (9),1686–1695年。https://doi.org/10.1039/C5TB02174J (2016)。
王S. 等人。 通过链条柔韧性对生物相容性海藻酸盐基纳米纤维膜进行电旋转。卡博海德。波利姆。 230,115665 。https://doi.org/10.1016/j.carbpol.2019.115665 (2020)。
Trinca, R. B., Westin, C. B., da Silva, J. A. F. 和 Moraes, Â. M. 电旋多层壳聚糖支架作为皮肤病变伤口敷料的潜在材料。欧洲波利莫杂志 88,161 –170。https://doi.org/10.1016/j.eurpolymj.2017.01.021 (2017)。
Wakuda, Y., Nishimoto, S., Suye, S. 和 Fujita, S. 利用芯壳电自旋技术实现具有各向异性结构的原生胶原水凝胶纳米纤维。科学报告 8 (1), 6248。https://doi.org/10.1038/s41598-018-24700-9 (2018)。
董、X等人。 一个各向异性三维电纺微/纳米纤维混合PLA/PCL支架。RSC高级研究。 9 (17), 9838–9844。https://doi.org/10.1039/C9RA00846B (2019)。
Cho, S. J., Jung, S. M., Kang, M., Shin, H. S. 和 Youk, J. H. 通过电旋处理PCL/PVP-b-PCL嵌段共聚物制备亲水性PCL纳米纤维支架,以增强细胞生物相容性。《聚合物》 69,95 –102。https://doi.org/10.1016/j.polymer.2015.05.037 (2015)。
Contardi, M. 等人。 含有羟基肉桂酸衍生物的电旋聚乙烯吡咯酮(PVP)水凝胶,作为潜在的伤口敷料。化学工程杂志 409,128144 。https://doi.org/10.1016/j.cej.2020.128144 (2021)。
Evrova, O. 等人。 杂交随机电纺聚(乳酸-共乙醇酸):聚(乙烯氧化物)(PLGA:PEO)纤维支架,增强肌母细胞的分化和排列。美国化学学会应用类物质。界面 8 (46), 31574–31586。https://doi.org/10.1021/acsami.6b11291 (2016)。
Rahmati, M. 等人。 组织工程应用中的电纺。《材料科学进展》。 117,100721 。https://doi.org/10.1016/j.pmatsci.2020.100721 (2021)。
张B. 等人。 无溶剂电纺:机遇与挑战。《Polym. Chem》杂志。 8 (2),333–352。https://doi.org/10.1039/C6PY01898J (2017)。
Vogt, L. 等人。 用于心脏组织工程的聚(ε-丙内酯)/聚(甘油乙酰胺)电旋支架,使用良性溶剂。科学工程 C 103,109712 。https://doi.org/10.1016/j.msec.2019.04.091 (2019年)。
波提翁迪,T. 等人。 肌肉骨骼组织3D生物打印的最新进展。生物制造 13 (2), 022001。https://doi.org/10.1088/1758-5090/abc8de (2021)。
Mu, X. 等人。 蛋白质基墨水3D打印的最新进展。波利姆科学进展。 115,101375 。https://doi.org/10.1016/j.progpolymsci.2021.101375 (2021)。
Fereshteh, Z. 7 – 用于三维支架工程的冻干技术。在功能性三维组织工程支架 中。(编者:邓、Y. 和 库伊珀,J.)151–174.https://doi.org/10.1016/B978-0-08-100979-6.00007-0 (伍德黑德出版社,2018年)。
Mondal, D., Griffith, M. 和 Venkatraman, S. S. 组织工程与药物递送中的多氯丙基生物材料:当前情景与挑战。国际杂志:波利姆。Mater。波利姆。生物材料。 65 (5), 255–265。https://doi.org/10.1080/00914037.2015.1103241 (2016)。
利托维琴科,J. 等人。 多功能生物支架开发的里程碑和当前成就。生物药剂。Mater。 6 (8),2412–2438。https://doi.org/10.1016/j.bioactmat.2021.01.007 (2021)。
Islam, S., Bhuiyan, M. A. R. 和 Islam, M. N. Chitin and Chitosan:生物医学工程中的结构、性质及应用。J. 波利姆。环境。 25 (3),854–866。https://doi.org/10.1007/s10924-016-0865-5 (2017)。
蒙达尔,A. 等人。 海藻酸钠-明胶水凝胶用于生物印刷NSCLC共培养的表征性与打印性。科学报告9 (1 ),19914年。https://doi.org/10.1038/s41598-019-55034-9 (2019)。
Tolg, C., Telmer, P. 和 Turley, E. 透明质酸寡糖的特定尺寸刺激成纤维细胞迁移和切除伤口修复。PLoS ONE 9 (2),e88479。https://doi.org/10.1371/journal.pone.0088479 (2014)。
Noh, I., Kim, N., Tran, H. N., Lee, J. & Lee,C. 3D可打印的透明质酸基水凝胶,其潜在应用为组织工程中的生物墨水。生物材料。研究。 23 (1),3。https://doi.org/10.1186/s40824-018-0152-8 (2019)。
张L. 等人。 近十年中丝绸支架在肌肉骨骼组织工程应用中的系统综述。ACS生物材料。科学工程。 7 (3), 817–840。https://doi.org/10.1021/acsbiomaterials.0c01716 (2021)。
李·J. M. 等人。 三维聚(ε-丙内酯)和丝纤维蛋白纳米复合纤维基质用于人工真皮。科学工程学 C 68 , 758–767。https://doi.org/10.1016/j.msec.2016.06.019 (2016)。
Suarato, G., Bertorelli, R., Athanassiou, A. 借鉴自然:生物聚合物与生物复合材料作为智能伤口护理材料。前面。生物工程师。生物技术。 6 . https://doi.org/10.3389/fbioe.2018.00137 (2018)。
Bedian, L., Villalba-Rodríguez, A. M., Hernández-Vargas, G., Parra-Saldivar, R. 和 Iqbal, H. M. N. 具有新特性的生物基材料用于组织工程应用:综述。国际生物学杂志。大环醇。 98,837 –846。https://doi.org/10.1016/j.ijbiomac.2017.02.048 (2017)。
扎姆里,M. F. M. A. 等人。 废弃物到健康:组织工程废弃物衍生材料综述。J. Clean。制作。 290,125792 。https://doi.org/10.1016/j.jclepro.2021.125792 (2021)。
Iravani, S. 和 Varma, R. S. 植物与植物基聚合物作为组织工程支架。绿色化学。 21 (18),4839–4867。https://doi.org/10.1039/C9GC02391G (2019)。
Joyce, K., Fabra, G. T., Bozkurt, Y. 和 Pandit, A. 天然生物材料的生物活性潜力:生物特性的鉴定、保留与评估。信号转导。目标。Ther。 6 (1),1–28。https://doi.org/10.1038/s41392-021-00512-8 (2021)。
伊拉斯托尔萨,A.,扎兰多纳,I.,安多内吉,M.,格雷罗,P. 和德拉卡巴,K。胶原蛋白和几胞菌的多样性:从食品到生物医学应用。食品水耕。 116,106633 。https://doi.org/10.1016/j.foodhyd.2021.106633 (2021)。
库尔卡尼,N. 等人。 肽-几百聚体为生物医学应用设计了支架。生物结合。化学。 32 (3), 448–465。https://doi.org/10.1021/acs.bioconjchem.1c00014 (2021)。
比利根,A. C. 等人。 组织工程中的植物基支架。ACS生物材料。科学工程。 7 (3), 926–938。https://doi.org/10.1021/acsbiomaterials.0c01527 (2021)。
金B. S.、达斯S.、张J. 和赵D.-W.用于组织和器官特异性微环境工程的去细胞外基质生物墨水。《化学评论》 120 (19),10608–10661。https://doi.org/10.1021/acs.chemrev.9b00808 (2020)。
Wösten, H. A. B. 用于酶、化学品和材料生产的丝状真菌。柯尔。观点。生物技术。 59,65 –70页。https://doi.org/10.1016/j.copbio.2019.02.010 (2019)。
Steinberg, G., Peñalva, M. A., Riquelme, M., Wösten, H. A., Harris, S. D. 菌丝生长的细胞生物学。在《真菌王国 》中。231–265.https://doi.org/10.1128/9781555819583.ch11 (约翰·威利父子有限公司,2017年)。
Antinori, M. E., Ceseracciu, L., Mancini, G., Heredia-Guerrero, J. A. 和 Athanassiou, A. 菌丝基材料的物理化学性质和生长动力学的微调。美国科学学会申请生物材料。 3 (2), 1044–1051。https://doi.org/10.1021/acsabm.9b01031 (2020)。
哈尼夫,M. 等人。 真菌菌丝的先进材料:物理性能的制造与调谐。科学报告 7 (1), 41292。https://doi.org/10.1038/srep41292 (2017)。
Ahmed, A., Narayanan, R. A. 和 Veni, A. R. 碳源复杂性对神经孢子体生物膜孔隙度、水分保持及细胞外基质组成的影响。《应用微生物学杂志》。 128 (4),1099–1108。https://doi.org/10.1111/jam.14539 (2020)。
Wasser, S. 药用蘑菇作为抗肿瘤和免疫调节多糖的来源。应用。微生物学。生物技术。 60 (3),258–274。https://doi.org/10.1007/s00253-002-1076-7 (2002)。
苏,C.-H。等人。 真菌菌丝体作为皮肤替代品的发展:对伤口愈合和成纤维细胞的影响。生物材料 20 (1), 61–68。https://doi.org/10.1016/S0142-9612(98)00139-2 (1999)。
钱,M.-Y。等人。 来自孢子囊形成延迟突变体的Rhizopus stolonifer菌丝床垫,作为促进伤口愈合的生物材料。PLoS ONE 10 (8),e0134090。https://doi.org/10.1371/journal.pone.0134090 (2015)。
Narayanan, K. B., Zo, S. M. 和 Han, S. S. 新型仿生几丁质-葡聚糖多糖纳米/微纤维真菌支架,用于组织工程应用。国际生物学杂志。大环醇。 149,724 –731页。https://doi.org/10.1016/j.ijbiomac.2020.01.276 (2020)。
Solari, P. 等人。 葡萄乾蝇黑腹泻的血清素神经回路失衡、超收缩肌肉活动和PD的线粒体形态PINK1B9被mucuna pruriens所挽救。《昆虫生理学杂志》。 111,32 –40。https://doi.org/10.1016/j.jinsphys.2018.10.007 (2018)。
琼斯,M. 等人。 真菌菌丝体及菌丝体的热降解与火灾特性:生物质复合材料。科学报告 8 (1),17583年。https://doi.org/10.1038/s41598-018-36032-9 (2018)。
张、X等。 热应激调节菌丝体生长、热休克蛋白表达、灵精酸的生物合成以及通过细胞质Ca2+的菌丝分支。应用:环境。微生物学。 82 (14),4112–4125。https://doi.org/10.1128/AEM.01036-16 (2016)。文章 CAS PubMed(出版医学) PubMed Central 谷歌学术
Yan, Z., Zhao, M., Wu, X., Zhang, J. 胸膜骨处理虫对持续热应激的代谢反应。前面。微生物学 ,10 。https://doi.org/10.3389/fmicb.2019.03148 (2020)。
Pera, L. M. 和 Callieri, D. A. 钙对真菌生长、菌丝形态及柠檬酸生成的影响 黑猪镄。叶状微生物学。(布拉格) 42 (6), 551–556。https://doi.org/10.1007/BF02815463 (1997)。
Qiu, Z., Wu, X., Gao, W., Zhang, J. 和 Huang, C. 高温诱导的菌丝体细胞壁完整性和结构破坏。应用。微生物学。生物技术。 102 (15), 6627–6636。https://doi.org/10.1007/s00253-018-9090-6 (2018)。
Chen, M., Patra, P. K., Warner, S. B. 和 Bhowmick, S. 纤维直径在电纺聚氯内酯支架上NIH 3T3成纤维细胞的粘附和增殖中的作用。组织工程。 13 (3), 579–587。https://doi.org/10.1089/ten.2006.0205 (2007)。
李、X等人。 不同直径排列和随机纤维对细胞行为的影响。胶体冲浪。B生物界面 171,461 –467。https://doi.org/10.1016/j.colsurfb.2018.07.045 (2018)。
Kennedy, K. M., Bhaw-Luximon, A. 和 Jhurry, D. 电旋聚合物支架中的细胞-基质机械相互作用:对支架设计与性能的启示。Acta Biomater。 50,41 –55页。https://doi.org/10.1016/j.actbio.2016.12.034 (2017)。
Bružauskaitė, I., Bironaitė, D., Bagdonas, E. 和 Bernotienė, E. 组织再生的支架与细胞:不同的支架孔径——不同的细胞效应。细胞技术 68 (3), 355–369。https://doi.org/10.1007/s10616-015-9895-4 (2016)。
Olvera, D., Schipani, R., Sathy, B. N. 和 Kelly, D. J. 在人类尺度上电纺高度多孔但机械功能强大的微纤维支架,用于韧带和肌腱组织工程。生物医学。Mater。 14 (3),035016。https://doi.org/10.1088/1748-605X/ab0de1 (2019)。
拉马纳坦,G. 等人。 将生物杂交纤维素醋酸酯-胶原蛋白双层基质制成纳米纤维海绵状敷料用于伤口愈合应用。生物大环醇 21 (6), 2512–2524。https://doi.org/10.1021/acs.biomac.0c00516 (2020)。
劳伦斯,M.;江,Y. 孔隙度、孔径分布、微观结构。载于《基于生物骨材的建筑材料:RILEM技术委员会最新报告236-BBM 》(主编:Amziane, S. 和 Collet, F.)RILEM最先进的报告;39–71.https://doi.org/10.1007/978-94-024-1031-0_2 (荷兰施普林格出版社:多德雷赫特,2017年)。
斯里达拉,S. S. 和 塔塔,N. R.一种利用滤光中测纳米纤维垫孔隙度的新方法。《工法:纤维杂志》。 8 (4),155892501300800420。https://doi.org/10.1177/155892501300800408 (2013)。
Ali, I. H., Khalil, I. A. 和 El-Sherbiny, I. M. 单剂量电旋纳米颗粒纳米颗粒纳米纤维,具有增强上皮化、胶原沉积和造粒特性。ACS申请学校。《界面》 8 (23),14453–14469。https://doi.org/10.1021/acsami.6b04369 (2016)。
Ameer, J. M., Pr, A. K. 和 Kasoju, N. 组织工程中调谐电旋支架孔隙度以实现有效细胞响应的策略。J. 功能。生物材料。 10 (3),30。https://doi.org/10.3390/jfb10030030 (2019)。
Gsib, O., Eggermont, L. J., Egles, C. 和 Bencherif, S. A. 基于大孔纤维蛋白的序列互穿聚合物网络用于皮肤组织工程的工程。生物材料。科学。 8 (24), 7106–7116。https://doi.org/10.1039/D0BM01161D (2020)。
罗萨里奥,T. 和 德西蒙,D. W.细胞外基质在发育与形态发生中的动态视角。生物学开发者。 341 (1),126–140页。https://doi.org/10.1016/j.ydbio.2009.10.026 (2010)。
埃德加,L. 等人。 组织工程中支架生物材料的异质性。材料学 9 (5),332。https://doi.org/10.3390/ma9050332 (2016)。
Girometta, C. 等。 通过 TGA 和红外光谱法对木材衰变物种菌丝体的表征。《纤维素》 27 (11), 6133–6148。https://doi.org/10.1007/s10570-020-03208-4 (2020)。
Bekiaris, G., Tagkouli, D., Koutrotsios, G., Kalogeropoulos, N. 和 Zervakis, G. I. 通过ATR-FTIR光谱和多变量分析评估葡聚糖和麦角甾醇中的Pleurotus蘑菇含量。《食品》 9 (4), 535。https://doi.org/10.3390/foods9040535 (2020)。
Naumann, A. 傅里叶变换红外(FTIR)显微镜与真菌成像。收录于《真菌学中的高级显微镜 》;真菌生物学(主编:Dahms, T. E. S. 和 Czymmek, K. J.),61–88页。https://doi.org/10.1007/978-3-319-22437-4_4 (施普林格国际出版社,Cham,2015年)。
Mazzon, G. 等人。 利用聚氨酯改性氨硅乳剂对棉织物织物进行疏水处理。应用。冲浪科学。 490,331 –342。https://doi.org/10.1016/j.apsusc.2019.06.069 (2019)。
Sun, W., Tajvidi, M., Hunt, C. G. 和 Howell, C. 全天然智能菌丝体表面,具可调节的润湿性。美国科学学会申请生物材料。 4 (1), 1015–1022。https://doi.org/10.1021/acsabm.0c01449 (2021年)。
Mader, M., Jérôme, V., Freitag, R., Agarwal, S. 和 Greiner, A. 超多孔、可压缩、可湿聚乳酸/聚丙内酯海绵用于组织工程。《生物大环》 19 (5),1663–1673。https://doi.org/10.1021/acs.biomac.8b00434 (2018)。
Papenburg, B. J., Rodrigues, E. D., Wessling, M. 和 Stamatialis, D. 关于材料表面地形和润湿性对细胞-材料相互作用作用的见解。《软物质》 6 (18),4377–4388。https://doi.org/10.1039/B927207K (2010)。
Bueno, E. M., Laevsky, G. 和 Barabino, G. A. 通过控流体动力学参数增强组织工程中支架细胞播种。J. 生物技术杂志。 129 (3),516–531。https://doi.org/10.1016/j.jbiotec.2007.01.005 (2007)。
詹森,E. J. P. 等人。 疏水性作为骨组织工程中聚合物支架的设计标准。生物材料 26 (21), 4423–4431。https://doi.org/10.1016/j.biomaterials.2004.11.011 (2005)。
舒尔特,V. A. 等人。 一种疏水全氟聚醚弹性体作为细胞培养和组织工程中可图案化的生物材料。生物材料 31 (33), 8583–8595。https://doi.org/10.1016/j.biomaterials.2010.07.070 (2010)。
Oh, S. H., An, D. B., Kim, T. H. 和 Lee, J. H. 广泛刚度梯度PVA/HA水凝胶用于研究干细胞分化行为。Acta Biomater。 35,23 –31。https://doi.org/10.1016/j.actbio.2016.02.016 (2016)。
Islam, M. R., Tudryn, G., Bucinell, R., Schadler, L. 和 Picu, R. C. 菌丝基颗粒复合材料的机械行为。科学杂志。 53 (24), 16371–16382。https://doi.org/10.1007/s10853-018-2797-z (2018)。
Ziegler, A. R., Bajwa, S. G., Holt, G. A., McIntyre, G. Bajwa, D. S. 由纤维素纤维制成的菌丝增强绿色生物复合材料的物理力学性能评估。农业应用工程 (2016年)。
霍尔特,G. A. 等人。 真菌菌丝体和棉花植物材料在生物降解模压包装材料制造中的应用:对部分棉花副产品混合物的评估研究。J. 生物基质土。生物能源 6 (4), 431–439。https://doi.org/10.1166/jbmb.2012.1241 (2012)。
Huan, S., Liu, G., Cheng, W., Han, G. 和 Bai, L. 电纺多(乳酸)基纤维纳米复合材料,由纤维素纳米晶体增强:纤维单轴排列对微观结构和机械性能的影响。生物巨环醇 19 (3), 1037–1046。https://doi.org/10.1021/acs.biomac.8b00023 (2018)。
黄L. 等人。 具有梯度孔隙结构和提升细胞渗透性能的丝部支架。《科学工程》杂志 94,179 –189。https://doi.org/10.1016/j.msec.2018.09.034 (2019)。
习,W.,Saw,T. B.,Delacour,D.,Lim,C. T. 和 Ladoux, B.。材料方法对主动组织力学的应用。自然牧师马特。 4 (1),23–44。https://doi.org/10.1038/s41578-018-0066-z (2019)。
吉马良斯,C. F.,加斯佩里尼,L.,马尔克斯,A. P. 和 雷斯,R. L.活体组织的刚性及其对组织工程的影响。自然牧师马特。 5 (5),351–370。https://doi.org/10.1038/s41578-019-0169-1 (2020)。
班纳吉,S.;Paruthy, S. B. 关于真菌代谢产物及其类似物作为抗癌剂的临床前与临床视角——从实验台到床边。在真菌代谢物 中。1–32 (2016).
Martínez-Montemayor, M. M., Ling, T., Suárez-Arroyo, I. J., Ortiz-Soto, G., Santiago-Negrón, C. L., Lacourt-Ventura, M. Y., Valentín-Acevedo, A., Lang, W. H., Rivas, F. 生物活性灵芝化合物的鉴定及体外中改良衍生物的合成,赋予抗癌活性。前面。药学, 10 。https://doi.org/10.3389/fphar.2019.00115 (2019)。
费雷拉,I. C. F. R. 等人。 灵芝多糖具有抗氧化、抗肿瘤和抗菌活性的化学特征。植物化学 114,38 –55。https://doi.org/10.1016/j.phytochem.2014.10.011 (2015)。
Attia, W., Bawadekji, A., Al Ali, K. 食用蘑菇 pleurotus ostreatus 菌丝提取物的抗氧化和免疫调节活性。南亚生物学研究杂志。 6,83 –91(2016年)。
庄,C.-M.等人。 仙地奇素,一种存在于明灵芝中的新型几丁-多糖共轭大分子:纯化、组成及性质。药学。生物学。 51 (1), 84–95。https://doi.org/10.3109/13880209.2012.711840 (2013)。
Radwan, F. F. Y., Perez, J. M. 和 Haque, A. 灵精酸的凋亡和免疫恢复效应为癌症补充治疗开辟了新的前景。J. 克林。Cell。免疫系统。 3 月3日,004年。https://doi.org/10.4172/2155-9899.S3-004 。(2011).
你,B.-J。等人 。利用固体培养基培养增强灵芝酸的生成及明明灵芝 的细胞毒性。生物科学。生物技术。生物化学。advpub. .https://doi.org/10.1271/bbb.120270 (2012)。
Frese, S. 等人。 心脏苷通过上调死亡受体4和5,在非小细胞肺癌细胞中启动Apo2L/TRAIL诱导的凋亡。癌症研究。 66 (11), 5867–5874。https://doi.org/10.1158/0008-5472.CAN-05-3544 (2006)。
Tracy, L. E., Minasian, R. A. 和 Caterson, E. J. 愈合伤口中的细胞外基质与皮肤成纤维细胞功能。《伤口护理》 5 (3), 119–136。https://doi.org/10.1089/wound.2014.0561 (2014)。
Mobasseri, R., Tian, L., Soleimani, M., Ramakrishna, S. 和 Naderi-Manesh, H. 生物活性分子改变表面增强了间充质干细胞的粘附和增殖。生物化学。生物物理学。Res. Commun. 483 (1),312–317。https://doi.org/10.1016/j.bbrc.2016.12.146 (2017)。
Rieger, K. A., Birch, N. P. 和 Schiffman, J. D. 设计电纺纳米纤维垫以促进伤口愈合:综述。《化学杂志》 B卷1 (36),4531–4541。https://doi.org/10.1039/C3TB20795A (2013)。