
Scan the WeChat code to contact us

Scan the WeChat code to contact us


摘要
本研究提出了一种新型的自生长、纤维状、天然复合材料,具有受控的物理特性,能够大量且覆盖大面积生产,基于真菌的主要体菌丝体。来自两种可食用药用真菌——灵芝和Pleurotus ostreatus——的菌丝体经过精心培育,通过两种生物底物提供营养:纤维素和纤维素/土豆葡萄糖,后者因成分中含有简单糖类,更容易被菌丝体消化。经过特定生长时间后,菌丝体会被处理以停止生长。根据其摄食底物的不同,最终的纤维结构在多糖、脂质、蛋白质和几丁质中的相对浓度不同。这些差异表现为形态和机械性能的变化。在纤维素上生长的材料含有更多几丁质,杨氏模量更高,伸长度较低,这表明当其摄食基底难以消化时,菌丝体材料会变得更硬。所有开发的纤维材料均为疏水性,水接触角大于120°。通过合理选择菌丝材料的养分基质来调整其特性的可能性,为其在各种规模应用中的应用铺平了道路。
介绍
材料化学和纳米技术已证明在开发具有任何期望性质的新材料方面具有强大能力,因为它们的协同作用可以在原子或分子层面工程化物质1,2,3,4.然而,生物体的繁殖能力在自然界中依然独一无二,材料工程无法复制。在材料科学和纳米技术中引入活体生物系统,以实现生物资源中可控开发的材料,这一策略正吸引着大量研究努力 5,6,7.这符合当今越来越重要的需求,即开发新的绿色和可持续材料,避免对地球造成污染8,9,10,11,12.事实上,合成塑料的全球环境降解问题 13,14与化石燃料枯竭问题相结合,推动材料相关研究转向可再生资源高分子材料的主要原因15,16,17.目前的研究重点集中在天然来源(如纤维素)中聚合物材料的开发18木质素19果胶 20,21来自植物,来自植物和动物的蛋白质 22,23,细菌聚酯24或者植物25等等,所有具有可持续性、生物相容性和可生物降解性质的材料 26,27.此类材料的开发通常需要对其生物源进行复杂且困难的处理方法,以进行提取、开发和功能化,这些方法可能成本高昂、耗时且产量低28.因此,尽管这些材料可能解决各种环境问题,但价格昂贵且用途有限 29,30.
克服这些问题的策略可能是开发在生长过程中性能可控和可调的复合生物材料,这些材料无需昂贵且复杂的加工方法即可使用。为了实现这一策略,我们选择了菌丝体,即真菌的营养下部。菌丝体已被确认是地球上最大的生物体(菌丝网络覆盖近10公里2在俄勒冈州的蓝山地区) 31,32.它生长是因为与养育它的物质共生关系,形成纠缠的分支纤维网络33图1A。纤维菌丝体的丝状体称为菌丝,由细长的细胞组成。这些细胞之间由内部多孔的交叉壁隔开,称为隔壁。并且全部被包围在管状细胞壁内,见图1B。细胞壁(图1C)在真菌形态发生中扮演多种生理角色,保护菌丝 34,35并为整个菌丝体提供机械强度36.它由几丁质、葡聚糖以及外层蛋白质如甘味蛋白和水臶蛋白组成37.菌丝的生长通过细胞膜和细胞壁在菌丝尖端的延伸实现。
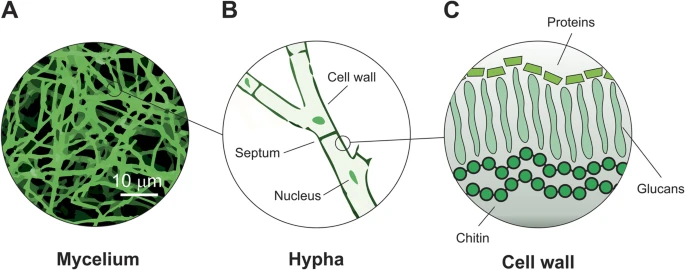
菌丝体主要由天然聚合物如几丁质、纤维素、蛋白质等组成,因此是一种天然聚合物复合纤维材料。由于其独特的结构和成分,我们预见将生产大量菌丝基材料。到目前为止,菌丝体主要被一家美国公司利用,该公司利用未加工的生物质被菌丝体粘合在一起,形成泡沫状结构38但菌丝体基材料仍有很大改进和进一步发展空间。
这项工作展示了菌丝体与不同成分多糖基底物的结合,以实现经过精心设计且具有可调节特性的纤维薄膜。使用了两种可食用药用真菌,分别是灵芝(G. lucidum)和Pleurotus ostreatus(P. ostreatus)。它们属于白腐菌类,能够分泌多种酶,其中一些酶还能降解难以水解的植物成分,如木质素。由于这两种物种含有重要的植物化学物质,科学界对其极大兴趣,但在本研究中,选择它们最重要的方面是它们能够分泌相似的酶,从而能够分解相同的底物,形成交织的丝状结构39,40,41.
如上所述,菌丝体通过物理压力和酶促分泌渗透进其摄食基质,将生物聚合物分解为易于吸收和运输的养分,如糖类。本研究所选的营养底物是纯纤维素和纤维素-土豆葡萄糖汤(PDB)生物聚合物,采用我们团队已发表的方法开发42.选择纤维素是天然聚合物最丰富的,而PDB是促进真菌生长的最常见介质,因为它富含易于菌丝体消化的简单糖。由于两种摄食底物的共同多糖特性,菌丝体预计会利用类似的真菌酶进行水解。此外,由于其开发方法的特殊性42这两种基底非常均匀,表面规则。这保证了菌丝体生长过程在恒定的营养平台上进行,从而使材料均匀。这两种供料基底非常适合证明已开发的纤维材料根据其供料基底调谐性能的能力,并且可作为其他更复杂基底的参考。本研究最有前景的结果是,开发的天然复合菌丝材料表现出可调节且高度受控的结构和机械性能,这通过利用不同的养分基底进行菌丝生长,从而证明菌丝材料的性质与其养分基质密切相关。研究发现,纤维菌丝材料在非晶纤维素上生长时机械刚性更高,杨氏模量更高,而非晶纤维素底物相比含有PDB的纤维素底物更难消化。此外,所有开发的纤维材料都表现出高度疏水性,这是天然材料难以实现的特性。
结果与讨论
1、形态特征
图2A展示了P. ostreatus菌丝体在纤维素基质上生长20天后的特征性物质。自生长的纤维膜覆盖了特定生长期后摄食基质的所有区域(直径9.5厘米的圆形区域)。正如预期,两种菌丝体在两种底物上的生长期完全相同,因为这两种菌丝体属于同一类白腐真菌,能够分泌相似的酶,且底物在两种基质中都富含多糖。尽管最终完全生长的菌丝体材料在所有情况下都呈现为纤维膜,如图2A所示,但它们在初始和晚期生长阶段的微观形态存在差异。
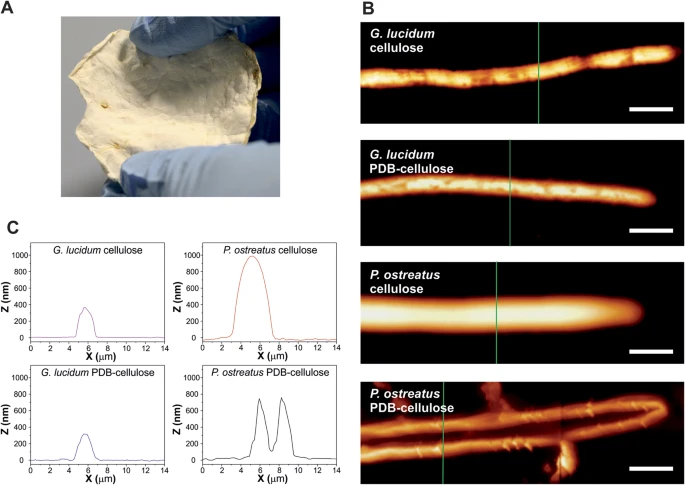
幼菌丝(2天大)菌丝(纤维菌丝体的丝状体)的形态特征通过AFM表征,见图2B和C。特征分析在菌丝尖端进行,以突出该阶段的差异。如图2B所示特征菌丝轮廓,P. ostreatus的菌丝直径通常比G. lucidum大,且不依赖于生长基质。两种情况下,菌丝相对平坦,宽厚比接近3。关于与生长基物的差异,可以看出在PDB纤维素和纤维素基物上生长的G. lucidum菌丝的形态非常相似。另一方面,底物的变化对P. ostreatus菌丝有强烈影响,因为它们在PDB纤维素底物上生长时,只有细胞边缘的细胞壁可见,这表明菌丝可能塌陷,这一现象将由扫描电子显微镜进一步分析。
图3A中通过SEM分析了自生长时间的表面特征。丝状物的密度随着生长时间明显增加,约20天后达到致密微孔结构。具体来说,G. lucidum的薄膜在每个生长阶段都显示了两种结构:管状和丝状。短且高度纠缠的管状结构在生长初期更为常见,但随着时间推移,致密丝状结构的存在会增加。还可以看到,致密丝的直径几乎不变。20天后,两种供料基底上生长的丝状体直径无显著差异,见图3B。更具体地说,G. lucidum 纤维薄膜在纤维素和纤维素-PDB底物上生长时的平均丝宽为0.8微米。另一方面,P. ostreatus薄膜呈现出一种独特的压缩丝状结构,见图3A。在这种情况下,丝状物的宽度明显取决于送料基底,当薄膜在纤维素上生长时,其数值比纤维素-PDB基底更高,见图3B。对于后者,菌丝丝在中央部分呈塌陷,这一现象已在AFM中观察到(见图2B),这种塌陷很可能导致其宽度相较纤维素生长的丝状物更短。内部静水压(膨胀力)为菌丝提供机械支撑,同时通过促使细胞质向菌丝尖端的质量流动,促进菌丝生长43.细胞壁防止菌丝因内部静水压而渗透溶化。当菌丝体在60°C下通过热处理停止生长2小时时,其丝状体不再受内部静水压支撑,因此在AFM和SEM图像中,尤其是P. ostreatus,它们看起来扁平。G. lucidum 丝状体更小,因此其结构不受热处理影响较小。生长在PDB-纤维素上P. ostreatus丝状体的中心塌缩可以通过其化学性质来评估,这部分将在下文关于ATR-FTIR测量的部分中讨论。

2、化学表征
采用ATR-FTIR光谱法表征自生长菌丝纤维薄膜的化学性质,发现它们因不同的进食基质存在重要差异。图4A显示了生长20天后四种不同样品的典型ATR-FTIR光谱。一般来说,菌丝体的红外吸收光谱与组成菌丝体的生物分子相关,例如脂质(3000–2800厘米)−1,约1740厘米−1)、蛋白质(酰胺I在1700–1600厘米处)−1,阿米德II和III,1575–1300厘米−1),核酸(1255–1245厘米)−1),以及多糖类(1200–900厘米)−1) 44,45.表1展示了采样的详细波段分配。
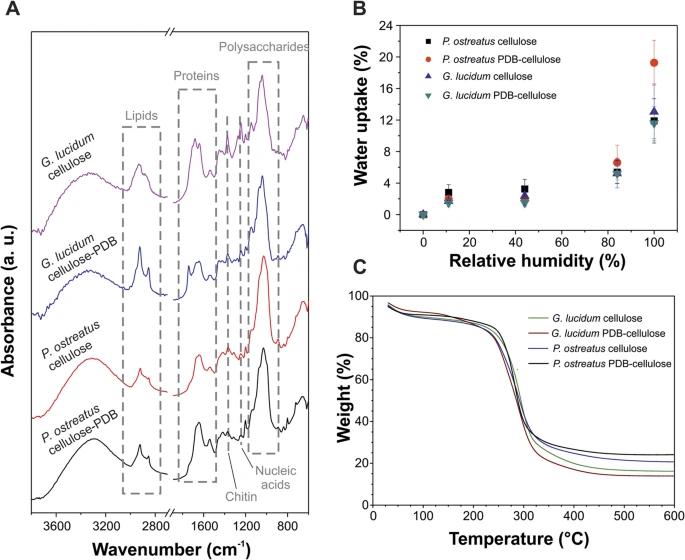
表1 红外光谱中观测到的波段(3800–600厘米)−1)在不同摄食基底上生长的菌丝体样本中。
| 编制 | 波数(厘米)−1)(强度)一个 ) | ||||
|---|---|---|---|---|---|
| G. lucidum 纤维素 | G. lucidumPDB-纤维素 | P. ostreatus 纤维素 | P. ostreatusPDB-纤维素 | 菌丝组分(主要贡献) | |
| O-H拉伸 | 3360(s) | 3342(s) | 3315(s) | 3294(s) | 多糖 |
| CH2非对称拉伸 | 2932(男) | 2926(s) | 2922(男) | 2924(男) | 脂质 |
| CH2对称拉伸 | 2855(米) | 2855(s) | 2855(米) | 2853(公) | 脂质 |
| 酯C=O拉伸 | 1743年(婚姻) | 1736年(左,西) | 1734年(SH,W) | 脂质 | |
| 阿米德I(β转) | 1686年(婚姻) | 1668年(婚姻) | 1670年(男) | 1670年(男) | 蛋白质 |
| 阿米德I(β页) | 1643年(m) | 1645年(m) | 1645年(m) | 1645年(m) | 蛋白质 |
| 阿米德二世 | 1545年(西) | 1543年(西) | 1543年(西) | 1543年(西) | 蛋白质 |
| CH2弯曲 | 1452年(m) | 1454年(男) | 1454年(男) | 1454年(男) | 脂质 |
| C-H弯曲 | 1375(西) | 1373年(西) | 1371年(西) | 1371年(西) | 甲壳 |
| 阿米德三世 | 1275(西) | 1282(西) | 蛋白质 | ||
| 邮局2–非对称拉伸 | 1248(西) | 1248(西) | 1252(西) | 1248(西) | 核酸 |
| C-C拉伸 + C-O 拉伸 + C-H 变形 | 1202(西) | 1202(西) | 1202(西) | 1202(西) | 多糖 |
| C-O…氢拉伸 | 1148(西) | 1148(公) | 1142(sh,m) | 1134(SH,M) | 多糖 |
| C-O拉伸 | 1063(对比) | 1068(对比) | 1063(对比) | 1067(对比) | 多糖 |
| C-C拉伸 | 1044(对比) | 1042(对比) | 1030(对比) | 1030(对比) | 多糖 |
| 葡聚糖β异构体C-H弯曲 | 889(西) | 893(西) | 893(西) | 891(西) | 多糖 |
| 曼南乐队 | 800(西) | 800(西) | 800(西) | 800(西) | 多糖 |
比较两种菌丝体光谱的一个总体观察是,独立于摄食底物,G. lucidum 纤维薄膜显示出更高的脂质贡献,而 P. ostreatus 薄膜则显示出相对更强烈的多糖带。有趣的是,摄食基底的化学性质也导致菌丝膜红外光谱的明显变化。特别是在PDB-纤维素底物上生长的G. lucidum薄膜显示出脂质(CH2在约2930厘米和2855厘米处的非对称和对称拉伸模态−1分别是酯C=O拉伸振动,1743厘米−1相对于在纯无定形纤维素基底上生长的植物。一个大偏移(18厘米)−1,1686年至1668厘米−1)降低归属于β匝酰胺I的波数也受到赞赏。这是由于菌丝体成分在摄食基质变化时发生化学修饰,导致这些二级结构的分子环境发生变化46.此外,当使用PDB-纤维素喂养G. lucidum菌丝体时,几丁质的相对存在量也降低了。与C-H弯曲模式相关的吸收峰值强度比值(约1374厘米)−1)到多糖的C-C拉伸(约1043厘米)之一−1)从纯纤维素供给底物的0.3降至PDB-纤维素供料底物的约0.1。
对于P. ostreatus样本,在PDB纤维素上生长时,蛋白质和脂质含量相较于纯纤维素生长时检测到相对增加。确实,条带的比值为1645厘米−1(β层次级结构中的酰胺I)到1030厘米处的−1(多糖的C-C拉伸)纤维素为0.3,PDB-纤维素底物培养样品为0.5。此外,与G. lucidum类似,几丁质与多糖的比例(1371厘米)−1/1030厘米−1纤维素的数值从0.08降至PDB-纤维素的0.06。细胞壁刚性几丁质相对量的减少,很可能与菌丝纤维在纤维素-PDB基底上生长时中心区域塌陷有关,这一点由AFM和SEM观察到(图3A)。事实上,有报道指出,无法合成几丁质的真菌突变体在形态上发生了改变,且对渗透敏感47.
3、流体动力学和热机械特性
在菌丝纤维膜生长20天后进行了水分摄取测量,见图4B。所有薄膜对湿度都非常有抵抗力,能吸收少量水分。湿度在50%相对湿度下,吸收率较低(<4%),且与基质和起始生物无关。当相对湿度为85%时,摄取率略高,约6%,但各样品间仍无差异。最后,在100%相对湿度下,在PDB纤维素上生长的P. ostreatus吸收率最高,达到20%,而其他材料为12%至13%。在PDB纤维素上生长的P. ostreatus吸收值应与其不同的化学成分有关,尤其是细胞壁的相对还原可能导致其湿度敏感性。低水分吸收与自生长膜的疏水特性相符,G. lucidum 和 P. ostreatus 的 WCA 值分别为 (122 ± 3)° 和 (121 ± 2)°,且与摄食基物无关。如此高的WCA值可与真菌细胞壁最外层特定蛋白质(如甘露蛋白和疏水蛋白)的疏水性有关 48,49以及与薄膜纤维性质相关的样品微米粗糙度(见下文AFM部分)。对自生长纤维薄膜生长20天后的热重分析(见图4C)显示不同样品间无显著差异,降解步骤独特,从约225°C开始,接近300°C结束。 这种高降解温度证明了它们的热稳定性,拓展了其应用领域。此外,所有样品的炭渣残留物重量均显著,介于15%至25%之间。
4、机械表征
机械表征测试见图5,同时还展示了每种薄膜20天生长后的典型实验曲线(图5A)。应力-应变曲线较为线性,仅在纤维素供料材料中出现脆性破坏,前有部分弯曲,表明网络正在逐渐断裂。测量参数显示所有样本之间存在显著差异,包括真菌种类和底物。一般来说,P. ostreatus基材料比G. lucidum基材料更刚性,断裂处伸长较小。P. ostreatus相较于G. lucidum纤维薄膜的更高刚性,可以通过ATR-FTIR分析结果来解释,该分析显示前者材料中多糖含量更高。因此,G. lucidum 较大的拉长形与蛋白质和脂质成分的较多相符,这些成分可能作为增塑剂。
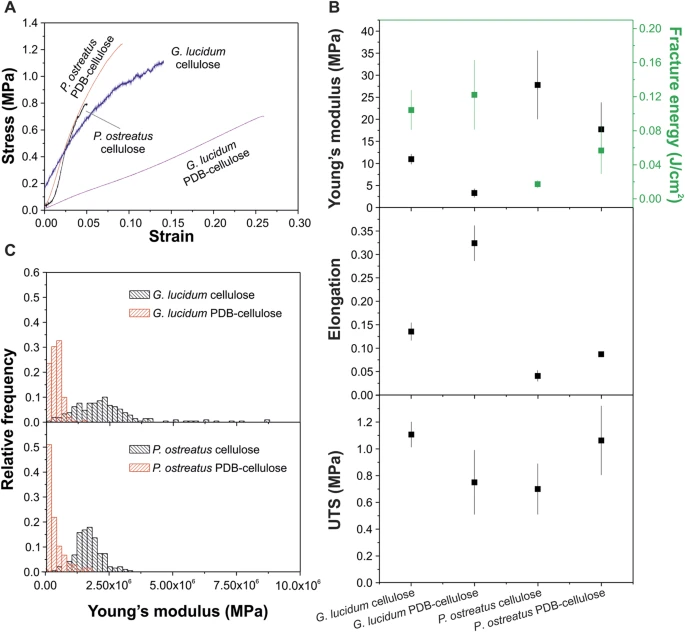
更换饲料底材也产生了类似效果,无论是对自生长菌丝材料的刚性还是延长,这自然源于它们不同的化学成分。特别是当PDB存在于摄食基质中时,菌丝体材料脂质或蛋白质含量较高,而几丁质含量较低。因此,加入富含糖的马铃薯葡萄糖汤,相比纤维素更容易被菌丝吸收,刺激增塑剂(脂质、蛋白质)的生物合成,减少刚性聚合物(几丁质)的生成,从而诱导菌丝体更高的延展性。
而极极强度则几乎不受材料来源影响,见图5B。通过断裂能(即强度和伸长度的结合)来估算其整体机械性能:这两种G. lucidum材料分别表现出更高的数值。这种行为归因于形态差异,G. lucidum 扭曲分枝结构的灵活性更大,使失败更为渐进,因此更平滑。
对2天前样品进行AFM压痕测量的机械结果见图5C。测量模数与宏观测试趋势相同,PDB纤维素供料材料系统性地比纯纤维素供料材料软,原因是脂质或蛋白质的增加,这些蛋白质可作为增塑剂,且前者中刚性几丁质的减少,正如FTIR研究所示。另一方面,杨氏模量分布值在G. lucidum和P. ostreatus中相似,尽管基于G. lucidum的材料在两种基底上都表现出更宽的杨氏模量分布。两种菌丝体在宏观测试中相似的杨氏模数值是主要区别,这可能归因于AFM凹陷的局部特征,测量受细胞壁影响,且在较小程度上受细胞内部结构影响,许多组成差异可能存在。AFM还用于评估已开发纤维材料的粗糙度,结果发现其粗糙度介于6000至7500纳米之间,除P. ostreatus外的所有生长材料的平均误差条值为1500纳米,其粗糙度达到10000纳米,很可能是由于菌丝中心部分塌陷所致。
5、菌丝膜与其他细菌自生长材料的比较
细菌纤维素和聚羟基烷酸酯(具体来说,是聚羟基丁酸酯或P(3HB))是两种有趣的生物聚合物,是石油基塑料的替代品 50,51这些可以被视为自生长的,就像菌丝体材料一样,因为它们是由微生物产生的。因此,我们在表2中比较了菌丝基薄膜与这些生物聚合物的主要特性。主要区别在于这三种系统的性质:细菌纤维素和P(3HB)是分子量极长的均聚物,而菌丝膜则是由多种生物聚合物(主要是脂质、多糖和蛋白质)组成的高分子复合材料。营养物质化学成分的变化会导致细菌纤维素和P(3HB)的最终产量及其分子量的差异。然而,对于菌丝膜来说,这些变化可以诱导生物聚合物相对贡献和形状的特异性改变,从而更好地控制最终性能。其他重要区别在于最终材料的纯化和分离方式。如上所述,菌丝体材料在生长结束时通过温和的热处理过程获得。另一方面,细菌纤维素通常通过多次在氢氧化钠热溶液中洗涤,然后在水中清洗至pH中性。对于P(3HB),纯化过程中使用有机溶剂作为氯仿。
表2 真菌纤维、细菌纤维素和聚(3-羟基丁酸酯)主要性质总结。
在机械性能方面,细菌纤维素和P(3HB)的杨氏模量和断裂应力值远高于真菌膜。然而,细菌纤维素的性质会根据其含水量变化,干燥时变得极其脆,难以作。这也反映在断裂伸长度上,而该延长值是细菌纤维素的最低值。P(3HB)在断裂处的伸长值介于纤维素生长和纤维素-PDB生长材料之间的差异,而G. lucidum材料(特别是用纤维素-PDB底物供给样品)的伸长值显著更高。因此,菌丝基材料比细菌纤维素和P(3HB)更软、更不脆,更易管理。
此外,菌丝膜为疏水材料,接触角高(高于120°)且吸水率低。P(3HB)接近疏水极限,接触角为89°,远低于菌丝纤维材料的接触角。相反,细菌纤维素表现出显著的亲水性,接触角值较低(~26°)。疏水性是本研究中介绍的菌丝材料的重要特性,因为强烈的亲水性和对水的敏感性是目前大多数工业化天然聚合物(如淀粉、纤维素)相较于传统合成聚合物的重要劣势,极大限制了其市场应用52.最后,菌丝体薄膜和P(3HB)的热稳定性相似(热降解温度约为300°C,与大多数汽油塑料相符)。细菌纤维素耐热性更高,降解温度为365°C。
6、结论
本研究中,我们制造了基于菌丝体的纤维薄膜,这些真菌属于同一类白腐真菌(G. lucidum 和 P. ostreatus),因此它们能够分泌相同的酶,并分解相同的天然聚合物以吸收并生长。菌丝体材料的生长是通过喂食两种天然聚合物基底完成的,即纯非晶纤维素和纤维素与PDB的混合物。摄食生物聚合物基质均质,保证菌丝体在整个生长过程中均匀吸收养分,从而形成均质菌丝体材料。两种营养底物均为多糖基底物,而含有PBD的基物因其在单糖中的浓度较高,菌丝体更容易吸收。在生长期结束时,菌丝膜经过热处理以停止生长并获得最终的纤维膜。
自生长薄膜的物理化学特性由两种植物的内在生理特征决定,最重要的是不同的摄食基质。事实上,PDB的存在影响了G. lucidum蛋白的二级结构,并导致G. lucidum基材料中脂质相对比例的增加、P. ostreatus蛋白的比例增加,以及两物种中几丁质的相对存在性降低。几丁质是一种刚性聚合物,在菌丝体细胞壁合成,以保护其丝状结构免受内部渗透压、外部湿度及其他化学和物理挑战的影响。在这项研究中,我们发现菌丝体在以纯纤维素为食时会合成更多几丁质。由于纤维素相较于PDB更难水解,且机械上更难穿透(详见补充图S1,了解两种供给基底的机械性能),菌丝纤维需要合成强硬的几丁质聚合物来完成此作用。
所有这些化学修饰都导致自生长菌丝材料机械性能的差异。当供料基底含有PDB时,自生长纤维材料的杨氏模量较低,断裂时伸长性增加,断裂能量也高于纤维素供料材料。因此,PDB的存在使菌丝体材料变得不那么刚性,更具有延展性。另一方面,所有样品均表现出高降解温度,表明它们在热上是稳定的。此外,这些真菌材料具有疏水性,水接触角较高,水分吸收值相对较低。这些特性对于许多小规模和大规模的应用都至关重要。
本研究中研究的纤维菌丝材料可以成为石油基塑料的现实替代品,具有细菌纤维素和P(3HB)等细菌产生的生物高分子的额外特征。鉴于许多发达国家正逐步采用可持续材料作为减少环境污染的策略,本文提出的这些新的菌丝基材料强烈支持这一策略。开发的菌丝体材料是天然聚合物复合材料(几丁质、纤维素、蛋白质等),生产所需能量最小(自生长),其特性可通过改变养分底质进行调谐。因此,这项工作能够为多种功能性菌丝材料的受控自我生长以低成本大量实现开辟道路。
方法
1、材料
99%的微晶纤维素(MCC)和三氟乙酸(TFA)均从Sigma-Aldrich采购并按原包装使用。马铃薯葡萄糖汤(PDB)以及灵芝和Pleurotus ostreatus真菌由美国宾夕法尼亚州立大学蘑菇产卵实验室提供,并在4摄氏度的黑暗中储存。
2、饲料基底的制备
制备了两种类型的供食底物,分别基于MCC和MCC与PDB的混合(1:1,w-w)。起始材料在60毫升玻璃瓶中以0.5重量%的TFA溶液中解出。为此,小瓶被用防腐剂封口,放入实验台上的摇床中3天,形成粘稠溶液。然后,将获得的溶液铸造在培养皿中,并置于化学罩中,直到溶剂完全蒸发(通常3-4天),最终获得独立薄膜。这两种摄食底物分别称为“纤维素”和“PDB-纤维素”。
3、菌丝膜的生长
所有材料和供料基材在使用前均以120°C高压灭菌(SYSTEC VX-40)保存15分钟。随后,将一小批菌丝体(G. lucidum 或 P. ostreatus)接种剂固定在不同的摄食基质上,以促进菌丝体的萌发。在菌丝接种物固定处滴入5微升PDB培养物,以促进菌丝体生长的启动。所有接种底物均在植物生长室(Memmert)中以25–30°C、70–80%相对湿度培养,孵育20天(除非手稿另有说明)。生长过程结束时,将形成的菌丝纤维材料放入60°C的烤箱中烘烤2小时,以抑制进一步生长。在进一步测试前,菌丝纤维膜会被轻柔地从其生长基底中取出。
4、形态学和局部力学特征
在扫描电子显微镜(SEM)的表征中,采用了JEOL JSM 6490LA显微镜,采用15 kV加速电压。在SEM评估之前,样品被镀上了黄金。然后,采集到的样品被安装在铝制支架上,并用双层碳胶带固定。
在磷酸盐缓冲盐水(PBS)液体环境中,通过原子力显微镜(AFM)对单根菌丝纤维进行了表征。采用了安装在Axio Observer D1(德国卡尔蔡司)倒置光学显微镜上的Nanowizard III AFM头(JPK仪器,德国)。采用V形DNP氮化硅悬臂(美国马萨诸塞州布鲁克),标称弹簧常数为0.24 N/m,空气共振频率范围为40 kHz至75 kHz,尖端典型曲率半径为>20 nm。每个悬臂梁的弹簧常数通过热噪声法现场测定。图像采用定量成像(QI)模式拍摄。样品施加了最大7 nN的力,每张图像采集了256×256 力-距离(FD)曲线。随后,FD曲线转换为力压入(FI),并通过赫兹拟合从曲线斜率中提取刚度。
5、化学表征
样品的红外光谱通过衰减全反射(ATR)附件(MIRacle ATR,PIKE Technologies)与傅里叶变换红外分光光度计FTIR光谱仪(Equinox 70 FT-IR,Bruker)结合获得。所有光谱记录在3800至600厘米之间−14厘米−1分辨率,累计128次扫描。在典型测量中,样品被轻轻放置在ATR附件的位置,缓慢压制。为确保获得光谱的可重复性,测量了每种类型的三个样品。
6、流体动力学表征
接触角(CA)量角仪(DataPhysics OCAH 200)用于室温静态水接触角测量。每滴液体的5微升液滴沉积在相应表面,1秒后拍摄滴体的侧面图像。CA通过拟合捕获的滴形自动计算。对每个样本在随机位置进行了多达15次接触角测量,并报告了其平均值和标准差。
为了取水,干燥样品会用灵敏的电子天平称重,然后放入不同的湿度箱中。样品通过干燥器调制数日进行干燥。设置的湿度条件为:0%、15%、45%、85%和100%。在湿度舱中放置数天后,每层膜被称重,并根据初始干重计算吸附水量。
7、热重分析
使用TGA Q500(TA仪器)进行热重分析(TGA),分析纤维薄膜的热降解行为。测量在铝盘中,含惰性氮的5–8毫克样品进行2大气层,流量为50毫升/分钟,温度范围为30至600°C,加热速率为5°C/分钟。体重下降及其导数同时被记录为时间/温度的函数。每个样本进行了三次重复。
8、机械表征
样品的机械表征在双柱通用测试机(Instron 3365)上完成。从样品生长20天后切割出宽4毫米、长25毫米的条状矩形条,厚度在0.1至0.3毫米之间,安装在机器夹具上。样品以每分钟2毫米的速度变形,直到失效。从应力-应变曲线中提取了杨氏模量E、极极拉伸强度UTS和断裂处伸长。断裂能量计算为每条曲线下方的面积。每个样品进行了六次测量以确认拉伸测试的可重复性,结果以平均值和标准差形式报告。所有测试均在室温23°C下进行。
附加信息
如何引用本文:Haneef, M. 等。《真菌菌丝的先进材料:物理性质的制造与调谐》。科学报告 7, 41292;doi: 10.1038/srep41292(2017)。
出版者注:施普林格自然在已出版地图和机构隶属关系中的管辖权主张方面保持中立。
参考文献
作者信息
作者与隶属关系
贡献
I.S.B.,J.A.H.-G.A.A.则构思了这项研究并设计了实验。J.A.H.-G.A.A.撰写了主要手稿文本。M.H.负责形态、热学、化学和润湿性表征。L.C.和C.C分析了样品的机械性能。所有作者都撰写了其能力的实验部分,并对手稿进行了审阅。
本研究被引用