
Scan the WeChat code to contact us

Scan the WeChat code to contact us



摘要
塑料污染正成为当今全球最严重的问题之一。另一方面,聚合物是非常多用途的材料,其产物无法完全消除,但必须找到替代方案。一个非常有前景的候选植物是真菌菌丝体。它是一种自生长的天然材料,由组织良好的天然聚合物组成,其形态、流体动力学和机械性能可以通过改变生长基底来调节。本研究表明,即使是对标准真菌生长介质——马铃薯葡萄糖汤(PDB)成分的微小调整,也能诱导灵芝菌丝体在形态、化学和流体动力学性质上的显著差异。菌丝体的生长速度也受到生长基质的影响。在富含d-葡萄糖的PDB中生长的菌丝体材料高度多孔、更厚,且比含少量木质素的PDB培养的菌丝体材料更容易吸附水分。而后者生长速度非常快,呈同心圆排列,密度更高且亲水性较低。然而,所有菌丝体均为疏水性,接触水的角度约为120°。菌丝体具有有趣的特性,在纳米尺度上可调谐,因此适用于多种应用:本研究所用方法可应用于不同菌株和条件,从而为各种用途选择最佳菌丝基材料。
介绍
2017年,全球塑料(即石油基聚合物)产量达到3.48亿吨,(1)其中近一半用于包装,使用寿命仅为一天。(2)因此,塑料生产不仅因为每年所需的原材料数量而不可持续,更重要的是,因为大约79%的塑料物品在使用寿命结束时最终被送往垃圾填埋场或海洋,对地球造成了严重影响。(3)因此,急需塑料材料的替代品,包括基于可再生或废弃资源的生物基、可降解材料。(4)
在此背景下,菌丝体基材料正逐渐成为有前景的生物材料。(5,6)菌丝体是由细长的细胞组成的网络,称为菌丝,真菌在地下或有机基质和土壤中扩展以获取养分。(7,8)菌丝体获得的材料经过低能处理以停止其生物活性后,既可生物降解,又采用循环经济理念开发,因为菌丝体可以在多种基底上生长,甚至是废弃物或难处理的基质。(9,10)尤其是白腐菌菌丝体,能够通过分泌具有多种功能的酶,完全分解木质素(11)并且可能最适合将废弃基底转化为新的可用材料。其他生物体也被用于生物材料的生产。例如,细菌可以在各种有机基质上生长,生成聚羟基烷酸酯或细菌纤维素。聚羟基烷酸盐的主要限制在于它们是在细胞内产生;因此,它们的净化过程漫长且昂贵。(12)细菌纤维素片形成于细胞外,但其多样性不及菌丝体,因为能够分泌纤维素的细菌必须在液体培养基中培养,而菌丝体也能在固体基底上生长,从而扩大了可能的培养基范围。此外,使用多种真菌菌株的可能性扩大了从结构到机械等多种特征的覆盖范围,这些特征均覆盖在菌丝基材料中。菌丝基材料的特性不仅取决于菌株,还受其他变量影响,(13)比如生长介质和条件。(14)然而,菌丝体作为生物材料最令人惊讶的特征是疏水性和耐高温能力。(15)这些特征主要源于菌丝体细胞壁中存在的几丁质,这种多糖与虾和昆虫的背甲中相同。与聚羟基醇酸酯和细菌纤维素不同,菌丝体实际上由干细胞壁组成,因此它们不仅仅是聚合物,而是脂质、多糖(如甘露糖)、几丁质和蛋白质(如水膋素)的复合体。(16)
近年来,基于菌丝体的材料被提出并研究用于建筑到纺织品等多种用途。(17,18)在这些工作中,真菌生长在农业废弃物上,并分析整个生物复合材料(被基底中掺入的菌丝体)的性质。(19)菌丝体很少被研究为独立多孔材料,脱离基质。菌丝网络本身仅从数学角度进行研究(20,21)或用于理解真菌生理学,(22)尤其是在发酵系统中。(23)不过,我们团队之前的一项研究(15)已经证明,即使是菌丝体本身,不嵌入生物复合材料中,作为独立材料也表现出良好的性能,但这些材料会根据生长介质而变化。
本研究的目标是进一步研究这一方面,特别是研究进食基底的轻微变化如何决定变化,从而调谐菌丝体的形态、化学成分、流体力学和机械性质。(24)特别是,我们将灵芝培养在标准真菌培养基——马铃薯葡萄糖汤(PDB)中,加入d-葡萄糖或碱性木质素,目的是分别提高最终菌丝体的亲水性和疏水性。d-葡萄糖因单糖而被菌丝体同化,且已存在于PDB中,且与其他更复杂的多糖一同存在。碱性木质素是木材中复杂分子的部分水解版本,但据报道其功能等效于原始分子,因为它使用相同的酶且在相似时间内代谢。(25)由于含有大量芳香族,菌丝体的分解较少。我们观察到,添加葡萄糖会形成更易吸附水分的菌丝体,同时因为它们更为多孔。而培养基中少量木质素则使菌丝比标准PDB更快且从接种物向同心生长,而不会形成大量稀疏菌落。此外,含有木质素的样本较薄且密度较高,而富含d葡萄糖的培养基中形成的菌丝体则更厚且更具柔韧性。现有结果证明,菌丝体摄食介质的微小变化也能精细调节最终菌丝材料的结构,即使在微观和纳米尺度上,还能调节其物理特性,预见到电子学的应用(26)生物技术。我们证明,调谐可以在“纯”菌丝体上进行,即菌丝体从其生长介质中移除,无需任何基因或机械工程(27)而且无需等待饲料基质的全部消化。(28)
材料与方法
1、化学品
从默克公司购买了土豆葡萄糖汤(P6685)、葡萄糖(G7021)和碱性木质素(471003)。
2、应变、培养基与生长条件
明灵芝DSM9621活性培养物从德国DSMZ购入,保存在100毫米培养皿中,培养基为马铃薯葡萄糖汤(PDB),每30天将培养基转移到新鲜培养基。一块培养20天的菌丝体被接种在100毫米培养皿中,培养皿内含有30毫升PDB 24 g/L(P培养基)、PDB 24 g/L加30 g/L的D-葡萄糖(G培养基)或PDB 24 g/L含碱性木质素2 g/L(L培养基;表1)。所用的PDB培养基组成是默克建议的标准配方。在选择最佳配方之前,明心灵芝在PDB中以不同浓度的d-葡萄糖和碱木质素培养(表S1).测试的d-葡萄糖浓度总是低于水中的葡萄糖溶解度极限(909 g/L),但远高于标准高葡萄糖细胞培养基(通常约5 g/L)中的浓度,范围在5到50 g/L之间。任何测试浓度下生长良好,选择了中间浓度。碱性木质素的浓度测试范围为0.2至10.0克/升,因其在水中的溶解度极限未被报告。在浓度高于5 g/L时,G. lucidum的生长严重受损,因此选择了中间浓度。水是所有介质的溶剂,所有介质使用前都经过高压灭菌处理。菌丝体在气候室(Memmert,HPP 260)中孵育,环境为27°C,水湿度为78%,且在黑暗中。每7天,共计28天,会采集对应每种情况的五个菌丝体,并用刮刀从基质上清除。菌丝体随后在50°C的烤箱中烘干15小时,随后进行进一步分析。
表1。本研究所用基物主要成分的标签及其相对含量(百分比重量)
| 标签 | 底物组成 | PDB % wt | D-葡萄糖百分比 wt | 碱性木质素 % wt |
|---|---|---|---|---|
| P | 土豆葡萄糖汤 24克/升 | 100 | 0 | 0 |
| G | d-葡萄糖 30 g/L + PDB 24 g/L | 44.4 | 55.6 | 0 |
| L | 碱性木质素 2 克/升 + PDB 24 克/升 | 92.3 | 0 | 7.7 |
3、生长速率与形态评估
菌丝体面积通过ImageJ软件测量,测量由尼康相机(Nikon)每天拍摄的照片。面积值相对于每个接种物的初始表面进行了归一化。干样品的重量采用分析天平测量。骨骼密度通过热科学Pycnomatic Evo氦核测测量法测量,厚度为4厘米3密室。测量在20°C进行。 样品的骨架体积,即孔隙无法进入气体时的体积,通过检测密封且压力平衡室内样品排挤的氦气体积引起的压力变化来测量。骨密度是通过样品质量除以骨架体积得到的。假设氦原子能够穿透菌丝体内所有开放孔隙。对同一样本进行了十项测量平均。孔隙度通过使用Pascal 140 Evo和Pascal 240 Evo汞孔隙测量仪(Thermo Fisher Scientific)进行的汞侵入孔隙测量(MIP)测定。汞侵入压力设定为0.0136兆帕,并持续增加至200兆帕,速率为每分钟6至14兆帕–1.汞与样品的接触角和纯汞的表面张力被假定为140°和0.48牛顿米–1,分别。使用沃什本方程计算施加压力的孔径,假设孔隙为圆柱形。测量时,样品被卷入专用膜分析支架中,并插入膨胀仪。通过扫描电子显微镜(SEM,JEOL JSM 6490LA)使用10 kV加速电压观察形态。观测过程中,样品被覆盖一层10纳米厚的金层,并用双层碳带固定在铝制短片上。
4、化学分析
样品的红外光谱通过衰减全反射(ATR)附件(MIRacle ATR,PIKE Technologies)与傅里叶变换红外分光光度计FTIR光谱仪(Equinox 70 FT-IR,Bruker)结合获得。所有光谱记录在3800至400厘米之间–1,直径4厘米–1分辨率,累计64次扫描。样品轻轻放置在ATR配件的一处,缓慢压制,将接触基底的部分(称为“底部”)或空气(称为“顶部”)压制,以区分两表面的化学成分。为确保获得光谱的可重复性,测量了每种类型的三个样本。光谱分析使用Origin pro 2016软件完成。元素分析仪使用元素分析仪(CNHS EA3000,欧矢量)进行。
5、流体动力学表面特征分析
接触角(CA)量角仪(DataPhysics OCAH 200)用于室温静态水接触角测量。在相应表面沉积了五微升的水滴,10秒后拍摄了水滴的侧面图像。CA通过拟合捕获的水滴形状自动计算。对每个样本在随机位置进行了多达15次接触角测量,并报告了其平均值和标准差。为了取水,干样品会用灵敏的电子天平称重,然后放入不同的湿度箱中。样品通过干燥器干燥24小时,称重后在100%湿度条件下再加24小时,最后再次称重。吸附水量是根据初始干重计算的。
6、机械特性
用Q800 DMA测试机(TA Instruments)测量了储存模量E′和棕褐色δ(即损失模数与储存模数的比值,代表相对能量耗散)。样品切割成20×35毫米2在室温下以单轴拉伸模式进行测试,施加振幅为20微米的正弦变形,频率为7、10和16赫兹。
结果与讨论
1、形态与生长参数
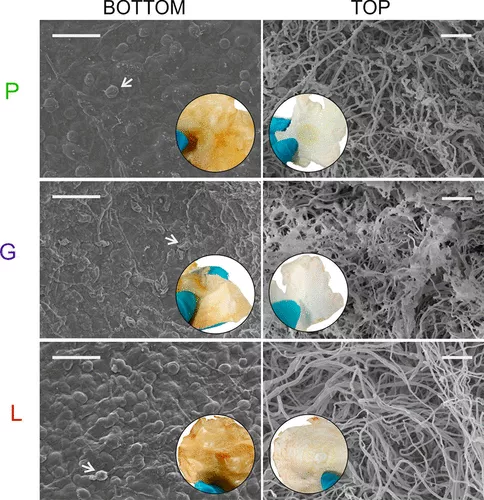
用相机拍摄的图像(图示1,圆形嵌套)和SEM图像(图示1菌丝体生长在不同摄食基质上(P,仅PDB;G、PDB和D-葡萄糖;L、PDB和碱性木质素,详见表1)如下所示图示1.在选择中间浓度前,测试了不同浓度的d-葡萄糖和碱性木质素,在这些条件下观察到灵芝的最佳生长。样品的两侧表现出显著差异:与饲料基底接触的一侧(“底部”)呈黄色,而另一侧(“顶部”)呈白色。此外,从扫描电子显微镜图像中可以看到,底部显示出大量孢子(由箭头指向图示1),而顶部则更为细丝状。除了这些属类差异外,还能观察到与摄食基质相关的其他差异。例如,在含有木质素的基底上生长的样本相比其他两种条件下生长的样本,菌丝网络更平滑且纠缠更少。使用我们之前工作中使用的相同定义,P生长样本既展现了短且高度纠缠的管状特征,也表现出细长的线状特征。(15)在G生长样本中,管状特征成为主导,而L生长样本则仅为细长的细线状特征。这些差异可以与不同类型样品生长模式的多样性有关,(29)可以在图示2一个。所有样本的生长均始于圆形接种。在P型,尤其是G培养基中,菌丝体通过形成随机分布的菌丝斑点进行,约10天后合并为一个斑点。而在L培养基中,则不会形成散布的“菌落”,而是初始接种物逐渐扩大,形成覆盖整个板块面积的更大斑点,20天内覆盖整个板块。这种不间断的生长促进了长丝状丝的形成。这些差异也影响菌丝体的宏观特征,因为在L培养基中生长的菌丝体表面可见同心的深色环(图示1,圆形内集)。
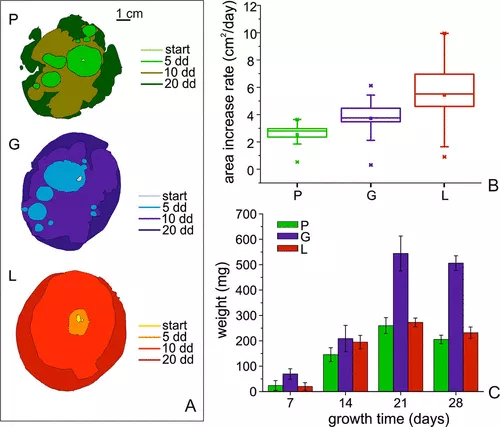
此外,菌丝体所占面积的增长速率根据其摄食介质变化,L介质中变化速度最高,达5.4±2.6厘米2P中等最低,最低为2.5±0.8厘米2/day (图示2B)虽然在L培养基中培养的菌丝体相对于其他培养基在进食培养基表面的扩展速度更快,但在培养基内的生长则不然。实际上,它们的最终体重在生长后3周内达到,约300毫克,与P培养基中菌丝体的重量非常相似。用G培养基培育的明心灵芝最终重量最高,为506 ± 28 mg(图示2C)所有培养基中所有样本的重量在生长3周后似乎都保持稳定。
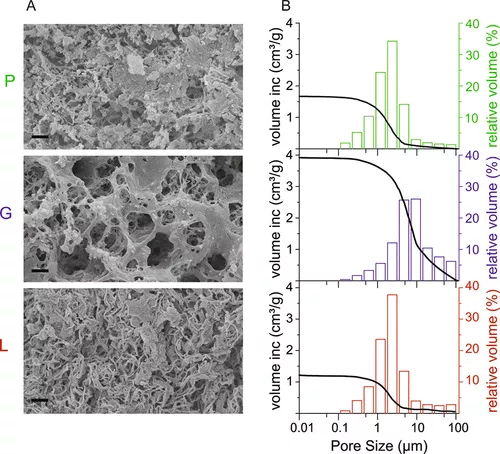
发育中的菌丝体样本具有多孔结构,并计算其骨骼密度。在L培养基中生长的样品([1.535 ± 0.005] g/cm,最高值3),而在P培养基中培养的菌丝体最低([1.342 ± 0.021] g/cm)3).G-中等生长的菌丝体呈现中间值([1.438 ± 0.014] g/cm3).G生长菌丝体在通过SEM和汞侵入孔隙测量分析时,孔径也比其他两种样品大(10至50微米)。图示3A,B)。对样品截面的SEM研究显示,较大直径的孔隙聚集在特定区域,可能是菌丝开始集中过量葡萄糖的地方。对于P型和L型生长的菌丝体,孔径分布在1到3微米之间。孔隙度和厚度的多样性与骨骼密度密切相关:G生长的菌丝体更厚且多孔(约占孔隙率的85%),图示3B,曲线);因此,它们的密度介于中等,而L生长的菌丝体则较薄且孔隙较少(约68%),图示3B,曲线),所以它们的密度最高。据我们所知,孔隙度从未被详细评估过基于菌丝的材料,但它是一个极具吸引力的特性,开启了广泛的应用。而且它可以通过调音,这更让人感兴趣。多孔材料在生物医学领域具有药物递送和组织工程等应用,并且在底物与催化剂相互作用的可能性得到验证后,可能成为酶固定化的平台。
培养基的生长速度、形态和化学成分之间的相关性并不直观,但可以假设,作为L,更难消化的培养基促使菌丝体分泌更多酶,从而决定了表面生长的宽广且快速,但总体积减少。另一方面,富含易于被菌丝体消化的化合物如d-葡萄糖,则允许在供食介质表面出现多个生长点,从而实现更深层的生长和最终增加物质的体积。菌丝形态的差异证实了这一假说:L培养基中观察到的较低分枝倾向可能表明菌丝体试图寻找营养更丰富的区域,而非由基质最佳消化引起的扩张。
2、化学特性
菌丝体样本通过ATR-FTIR光谱进行表征。(30,31)图示4A在不同生长时间和摄食基底下展现出一些具有代表性的菌丝体光谱。差异主要体现在每个峰的相对高度和贡献方面,在分析与空气接触时生长的菌丝体表面(顶部表面)时更为明显图示1).在分析与基底接触时生长的菌丝体表面,很难区分培养基与菌丝体的贡献,因此这些结果未被显示。一般来说,多糖的主要吸收(O—H拉伸模式,约3250厘米处)–1,在约1070厘米处的C—O拉伸模–1,在约1020厘米处的C—C拉伸模–1以及 C—H 弯模,位于 ∼895 厘米–1)、脂质(不对称和对称CH2拉伸模式分别位于2935厘米和2880厘米–1分别,以及 约1720厘米处的C═O拉伸模–1)、蛋白质(酰胺I和酰胺II,分别位于约1645厘米和∼1545厘米处–1以及几丁质(C—H弯曲模态,约1375厘米)–1)被识别。(15,32)菌丝体表面存在所有通常用于蛋白质和其他生物分子用于附着在生物表面的化学基团,进一步增强了利用菌丝体在生物技术应用中的可能性。从光谱中可得三种红外比值,即几丁质/多糖、蛋白质/多糖和脂质/多糖,这些比例对应于C-H弯曲模式强度比值约1375厘米–1,amide I 位于 ∼1645 厘米–1,以及非对称的CH2拉伸模式,2935厘米–1分别,其中一个C–C拉伸模态位于约1020厘米–1,是计算出来的,图示4B.对于PDB,14天到28天的比例几乎是重复的,表明在发育2周内,几丁质、蛋白质和脂质相较于多糖的相对增加。另一方面,对于G和L的供料底物,同期比值的增加幅度较小。然而,G底物的比值保持恒定低值,而L型底物的所有生长期均计算出较高的比值,菌丝体在P培养基中生长28天后才达到。这很可能与特定代谢途径的增减有关,这取决于获得的营养素。因此,来自G底物的d-葡萄糖可以直接参与碳水化合物代谢,增加细胞壁中的多糖含量,并保持上述描述的红外波段比率较低。(33)相比之下,L底物中的碱性木质素可以被去聚合成木质素单体,并由此参与许多其他生化途径,保持相较于其他多糖的几丁质、蛋白质和脂质的较高产能。(34,35)
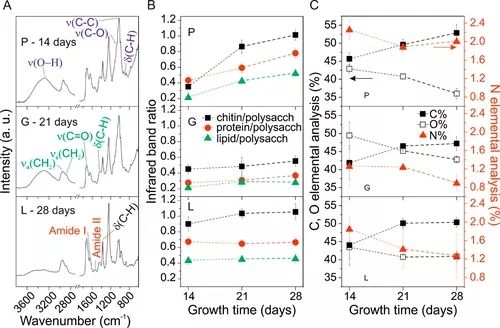
为进一步分析菌丝体样品的化学成分,会进行元素分析。图示4C报告不同日子和供料基底物中C、O和N的百分比。总体来看,C%(值在42%到53%之间)随着生长时间增加,而O%(范围在36%到50%之间)下降,N%(值在0.9–2.3%)保持恒定或略有下降。尽管整体趋势相似,N/C比值在G样本中最低,为0.019±0.002,P样本为0.038±0.001,L样本为0.025±0.008(数据未显示)。元素分析因此证实了红外带比已观察到的多糖和蛋白质生成差异。
3、流体动力学表征
流体动力学表征进一步证实了化学成分的差异。事实上,用G培养基生长的菌丝体比用L和P介质培养的菌丝体吸附湿度更高(图示5A)更具体地说,生长28天后采集时,G菌丝体可吸附其重量的58±10%,而L和P分别吸附31±3%和37±3%。这些G样品的结果可以解释为蛋白质和几丁质中多糖含量较强;因此,它们应具有相当的吸湿性。它们的高孔隙率,如图示3B,还能提升吸水能力。另一方面,不同菌丝体样品的水接触角值非常相似,表明所有样品均为疏水性,约为120°(图示5B)很可能化学成分差异不大,无法决定表面不同的行为。此外,疏水性高度依赖于表面粗糙度和表面存在的空气间隙,鉴于所有样品高度多孔的结构,空气层之间差异不大。(36,37)水分吸附在这方面更有参考价值,因为它不仅关注表面,还关注整体材料。疏水性结合孔隙性,表明菌丝体也可用作油吸和水-油分离的泡沫。还需要进一步研究渗透性和吸附能力。
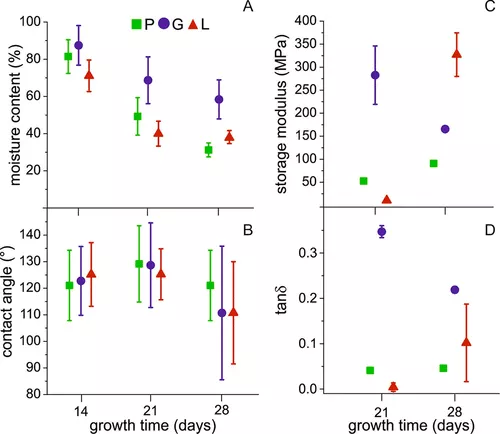
4、机械特性
显现样品的力学性质难以测量,因为菌丝体是纤维材料,由于纤维相对于力的随机方向,对应力的响应可能不同。此外,菌丝体在纤维分布、方向和厚度方面结构不均匀,这为机械响应增添了随机特性,尤其是在大变形和断裂初期。因此,常用的机械表征拉伸测试未能提供可重复的结果(图S1). 而动态力学分析则允许收集可靠数据,因为施加的应变较低(拉伸测试为<0.1%),因此局部不均匀性和纤维取向不会影响整体响应。使用DMA得到的结果(图示5尽管散布较大,但与菌丝体的外观和接触外观相关联。经过21天生长,G生长菌丝体拥有最高的储存模量和最高的能量耗散:其棕褐色δ确实是P菌丝体(0.041±±0.006)的十倍(0.347 0.013),也是L菌丝体(0.004 ± 0.009)的100倍。储存模量与材料以弹性方式储存变形的能力相关,而棕褐色δ与其阻尼性有关,(38)因此,G菌丝在生长时显得非常延展性强。然而,在生长28天后采集时,其储存模量从612±48兆帕降至283±63兆帕,褐色δ降至0。 219±0.007,因此它们开始变得更脆。另一方面,P菌丝体在采集时间内保持基本相同的机械特性,而L菌丝体在采集28天后,储存模数增加30倍,达到327±47兆帕,相较于之前采集。然而,由于G菌丝体的棕褐色较低,它们仍比G菌丝体更脆δ。这些结果表明,机械性能受采集时间影响较大,且由于难以预测,必须针对每种条件进行评估。尤其是G样本,是唯一随着时间推移变得更脆的样品。这可能是因为湿度对它们的影响更强。水确实具有塑化作用,且菌丝体的含水能力最高,如以下所述图示5一个。即使对于G样品,这一容量也会随着时间推移而减弱,同时影响观察到的机械性能。总体来看,其表面机械性能优于由聚羟基烷酸酯等微生物产生的其他常见生物聚合物(39)或细菌纤维素,(40,41)据报道,这些 Young 模数为 GPa 阶。(42)这主要是因为菌丝体不是笨重的聚合物,而是低密度网络:事实上,AFM对单根纤维进行的机械测量得到的数值远大于此。(15)此外,其化学成分并非均匀,而是由不同大分子组成,无法形成非常有序的结构。然而,考虑到上述观察到的葡萄糖的塑化效应以及通过将菌丝体与其他生物聚合物混合开发生物复合材料的可能性,这些特性可以很容易地调优。此外,菌丝体仍保持比其他生物聚合物更优的水动力学和热性能。
结论
本研究研究真菌菌丝体作为材料的性质发展与调谐,略微调整取食基底。我们证明,即使是常见真菌培养基成分的微小变化,也能决定菌丝体性质的显著变化。特别是,灵芝菌丝体在标准真菌培养基(P培养基)PDB上培养,并在添加d-葡萄糖或木质素(分别为G和L培养基)的PDB上进行培养,并比较了它们的结构、化学、流体动力学和机械性能。在L培养基中生长的菌丝体表面积膨胀更快,最终材料看起来密集且带有细长的丝状特征,而G培养基的菌丝体则多孔且最厚。正如预期的那样,G生长的菌丝体吸湿性也比其他菌丝体更强,在蒸汽饱和的大气中吸收更多水分。所有菌丝体的水接触角均可比,表明疏水材料的形成。尽管由于菌丝体结构不均,机械性质难以评估,但也受底物成分影响,尤其是葡萄糖量,使菌丝体更具延展性。机械性能是这些材料的一个重要弱点,且湿度被观察到最为重要,因此可以尝试葡萄糖和木质素的组合,以获得延展性强但孔隙较少的菌丝体。通过比较不同的灭活方法或改变生长条件,例如通过搅拌培养物改善其通气性,可以更精确地控制显微形态(例如孔隙度和密度)。这项工作清楚地展示了菌丝体作为未来可持续材料所能提供的无限可能性,适用于需要不同结构和性能材料的多种应用。
参考文献
本文参考文献 另外42篇出版物。